Somos expertos en Elastografía Hepática. Nuestro médico de cabecera el Dr Guillermo Pérez es Profesional especialista en medicina interna y gastroenterología con énfasis en enfermedades hepáticas entrenado en ultrasonido abdominal en la Escuela Latinoamericana de Ecografía Diagnóstica e intervencionista y con entrenamiento Certificado por Echosens Francia en Elastografía hepática Fibroscan con más de 500 estudios realizados con equipos de última tecnología apoyados por ultrasonido de alta resolución Doppler Color.
Elastografía Hepática de transición Fibroscan Bogotá
¿Necesita un especialista en elastografía hepática de transición?
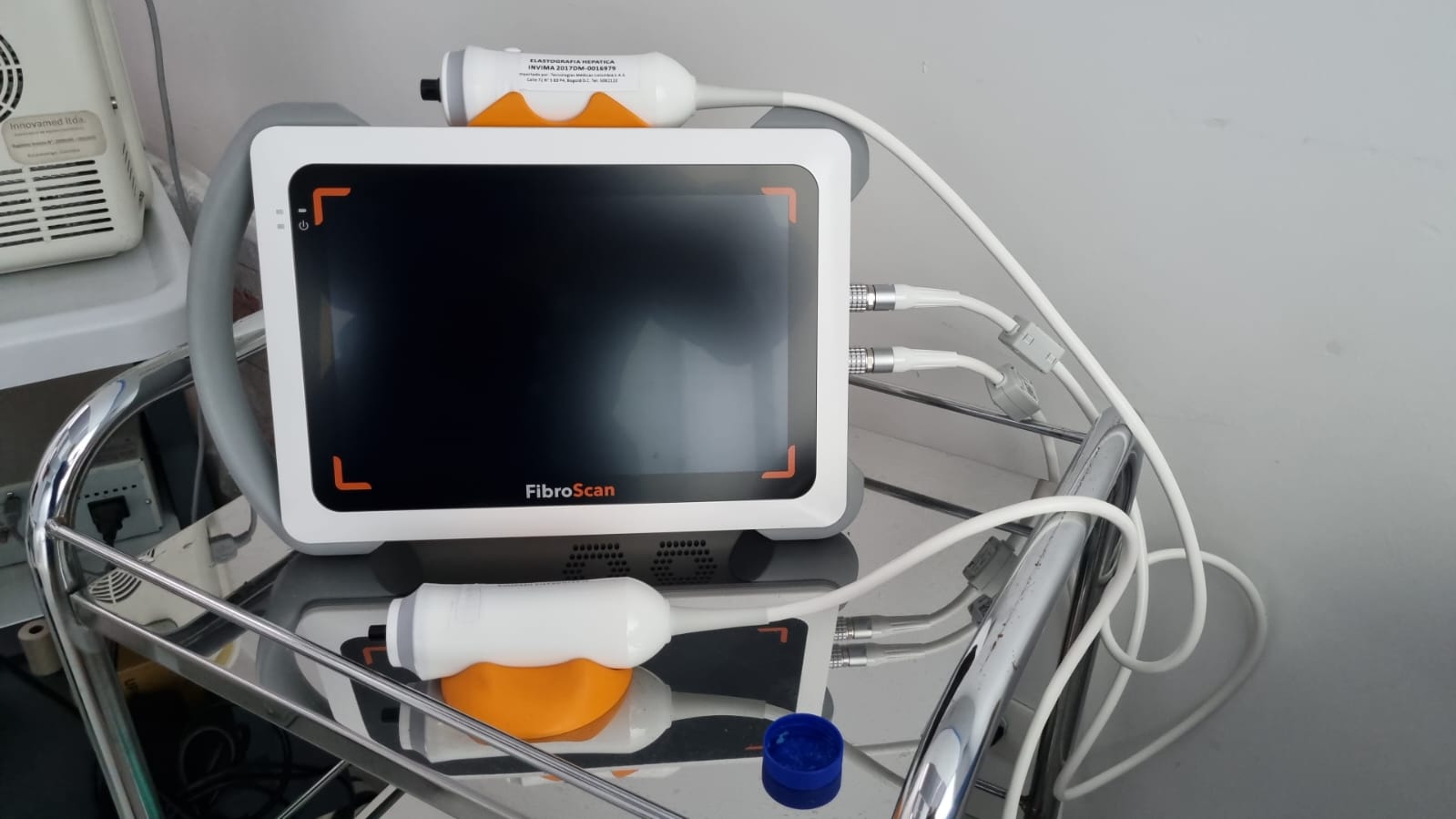
La elastografia hepática o Fibroscan® reemplaza hoy en día en la mayoría de los casos a la biopsia hepática ya que permite determinar con gran exactitud el grado de fibrosis que tiene el hígado o si hay cirrosis.
La velocidad de propagación de la onda de corte está directamente relacionada a la rigidez del tejido ( entra más dureza de los tejidos mayor es el corte de propagación) , la cual es medidas en Kilo Pascales ( kPa) . La exploración es rápido (5 minutos ) , reproducible y suministra información desde una porción mucho mayor de tejido hepático comparándolo a la biopsias hepática ( un cilindro de 1 cm de diámetro y una longitud de 4 cm, es 100 veces mayor que una biopsia hepática ). Esto hace que el riesgo de una muestra error es significativamente mucho más bajo . Los criterios de calidad de una medición fiable son al menos 10 mediciones válidas con una tasa de éxito de al menos 60% y un variación entre las mediciones (IQR/median) menor del 30%.
Limitaciones al intentar realizar mediciones : Costillas muy juntas , Obesidad grado II o III ( Debe utilizarse sonda XL ) Distancia entre la piel y la cápsula de Glisson mayor de 34 mm antes 24 mm).
Indicaciones:

MASLD: MASLD ó MetALD (Enfermedad hepática esteatótica asociada a disfunción metabólica)
Es un término nuevo para la enfermedad del hígado graso no alcohólico (EHGNA o NAFLD) y se refiere a la acumulación de grasa en el hígado debido a problemas metabólicos como obesidad o diabetes, pero sin consumo significativo de alcohol. Es la enfermedad hepática crónica más común en el mundo y su progresión puede llevar a inflamación, daño hepático y fibrosis, cirrosis y cáncer de hígado. La originan la Obesidad , Diabetes , Hipertensón arterial y el aumento de LDL Colesterol igual la hiperuricemia, el síndrome metabólico. Sin tratamiento puede progresar a inflamación , fibrosis cirrosis y cáncer hepatocelular siendo el grupo de mayor riesgo los obesos diabéticos no controlados

MASH:
Es la anterior asociada a un aumento de la transaminasas mas especifico de la AST o ALT lo cual refleja inflamación del tejido hepático ( Esteatohepatitis )
Tanto el MASLD como el MASH pueden ser asintomáticos o causas síntomas inespecíficos como fatiga , cansancio, astenia adinamia o disconfort o molestias abdominales no específicas.

Enfermedad hepática Mixta:
Se considera un grupo de pacientes que pueden presentar MASLD ó MASH Mixto metabólico y por consumo de Alcohol.
- Rangos de consumo de alcohol a tener en cuenta mayor de 50 Gr / semana en hombres ó de 60 Gr en mujeres
- Factor genético predisponente la presencia del Gen PNPLA3 el cual predispone a fibrosis progresiva y cirrosis.

Enfermedad hepática por Alcohol

Hepatitis Virales B y C

Hemocromatosis

Enfermedad de Wilson

Enfermedad de Wilson

Cirrosis Biliar Primaria

Hepatitis Autoinmunes Tipo I y II y hepatopatías autoinmune
Todas las anteriores se consideran indicaciones de Elastografias hepáticas , no obstante existen índices sewrológicos que pueden predecir e indicar subgrupos de pacientes de mas riesgos como el índice FIB4 cuando es igual o mayor de 1.3
FIB 4 = Edad ( años ) x AST/R.plaquetas x ALT

Procedimiento . Se realizan 10 mediciones espacio intercostal derecho línea media clavicular con un éxito minino de 60% resultado de kilopascales kPa. ( vn 0-6 kPa) . Para interpretarlo debe tenerse en cuenta el nivel de ingesta de alcohol y el componente metabólico . la IQR/Med debe estar menor de 30% para dar fiabilidad al resultado el cual se expresa un probabilidades .
FIB 4 = Edad ( años ) x AST/R.plaquetas x ALT
Este procedimiento consiste en un ultrasonido de 50 MHz montado sobre un transductor sobre un eje axial de vibración. En Bogotá este ecógrafo sofisticado permite determinar el grado de dureza del tejido hepático y así saber en que estadio o grado avanzado esta una enfermedad que afecte al hígado como son el higado graso no alcohólico o por alcohol , la obesidad con o sin diabetes , las hepatitis virales B y C y las enfermedades autoinmunes e incluso las hereditarias que estan asociadas al metabolismo del hierro y el cobre como la hemocromatosis y la enfermedad de Wilson.
La elastografia hepática o Fibroscan® reemplaza hoy en día en la mayoría de los casos a la biopsia hepática ya que permite determinar con gran exactitud que grado de fibrosis tiene el hígado o si ya esta cirrótico y así saber en que etapa va la enfermedad .
La velocidad de propagación de la onda de corte está directamente relacionada a la rigidez del tejido ( entra más dureza de los tejidos mayor es el corte de propagación) , la cual es medidas en Kilo Pascales ( kPa) . La exploración es rápido (5 minutos ) , reproducible y suministra información desde una porción mucho mayor de tejido hepático comparándolo a la biopsias hepática ( un cilindro de 1 cm de diámetro y una longitud de 4 cm, es 100 veces mayor que una biopsia hepática ). Esto hace que el riesgo de una muestra error es significativamente mucho más bajo . Los criterios de calidad a tener en cuenta una medición fiable son al menos 10 mediciones válidas con una tasa de éxito de al menos 60%. En adiciones, el rango intercuartil (IQR/median) de todas las mediciones validadas debe ser inferior a 30% del valor de la mediana. una de las limitaciones principales de la técnica es que en aproximadamente el 15-20% de los pacientes da resultados no interpretables, principalmente relacionados con la presencia de obesidad. Factores diferentes a la fibrosis podrían influenciar hasta 1.5 valores. La inflamación, colestasis y el hígado congestivo incrementa la dureza hepática.
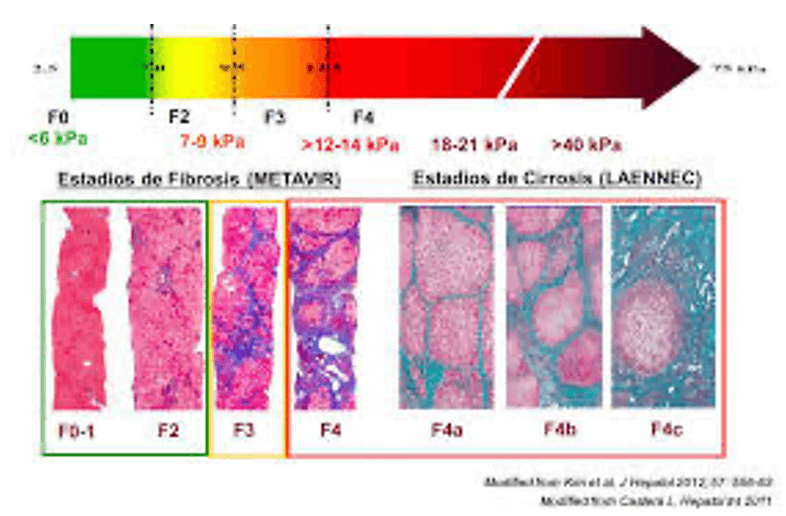
Probabilidad pos prueba de cirrosis ( prevalencia de cirrosis 14% ). Conforme a valores de FibroScan® de acuerdo a estudio de Dagos y colaboradores.
Dureza Hepática kPa Probabilidad post prueba de cirrosis
Menor de 7 Menor del 3%
7.1- 9.6 6%
9.7-12 18%
12.1-17 27%
Mayor de 17 72%
Ofrece varias ventajas una es na prueba no invasiva con 0% de complicaciones, rápida, reproducible y valora 100 veces más tejido hepático que la biopsia hepática.
En la Cr. 23 #124-87 consultorio 206 de la torre 2 en la ciudad de Bogotá . Para programar su cita comuníquese a los teléfonos Tel: (57) (601) 790 0643 | Cel: (57) 314 392 2455
- Esteatosis Hepática o Higado graso no alcohólico (link)
- Enfermedad hepática crónica por Alcohol
- Hepatitis C crónica
- Hepatitis B Crónica
- Hemocromatosis
- Hepatitis Autoinmune
- Citas oportunas el mismo día que la solicite o al día siguiente
- Experiencia somos pioneros del servicio más de 500 procedimientos realizados con una tasa muy baja de 2.8 fallidos
- Realizado por personal altamente calificado y con certificación de Echosens Francia.
- Correlación clínica patológica. Hemos superado con creces el volumen de procedimientos exigidos para este servicio.
- Apoyado por Ultrasonido abdominal . lo cual ofrece las siguientes ventajas al mismo tiempo y realizados por el mismo operados:
- Únicos con medición de distancia piel cápsula de Glisson con transductor lineal de 7.5 Hz, lo cual asegura el espacio intercostal óptimo.
- Determinación del grado de Esteatosis sin necesidad de usar concomitantemente el Cap.
- Detección de micronodularidad en la superficie hepática lo cual aumenta la sensibilidad del examen.
- Determinación diámetro longitudinal del Bazo que se relación con hiperesplenismo.
- Descartar presencia de ascitis en tiempo real, lo cual contraindica la realización del examen.
- Trato amable y cordial.
- Consulta especializada en Gastro-hepatología,
- La posibilidad de traslado de nuestro equipo a varios centros dado a su portabilidad.
- La presencia de Sonda XL al igual que la sonda M en un mismo equipo con software actualizado.
- Insuficiencia cardiaca congestiva
- Ingesta reciente de Alcohol
- Colestasis
- Ascitis
- Hepatitis Agudas
- La exploración inicial con el paciente en ayunas en decúbito supino y con el brazo derecho detrás de la cabeza. La sonda se aplica sobre la silueta hepática, entre las costillas, en la línea media axilar derecha y perpendicular al plano de piel. El explorados debe mantener la posición de la sonda ( con el mínimo movimiento posible ) y pulsar el botón para obtener 10 (diez) determinaciones válidas repetidas, con un IQR ó RIC (rango intercualítico ) o variación del ttal de mediciones válidas con respecto a su valor mediano y el valor final de rigidez o mediana de las 10 determinaciones válidas expreasado en kilopascales (KPa) menor del 30% y con mínimo 60% de las mediciones aceptables. En la pantalla del ordenador se genera una imagen de la onda elástica en 2 dimensiones y su morfología puede facilitar la obtención de registros válidos.
- El personal médico o no médico una enfermera puede realizar la exploración tras completar un corto aprendizaje (de50 a 100 exploraciones), pero la interpretación de los resultados la debe realizar un médico con conocimientos amplios sobre el paciente y las características y limitaciones de la técnica.
- Antes de interpretar una medición bien realizada debe conocerse la historia clínica del paciente que existen limitaciones en determinadas patologías que pueden dar valores en rangos muy por encima de la población sin ésas entidades. La elastografia de transición o FibroScan® puede verse influida ( especialmente en pacientes sin fibrosis F0 ó con fibrosis mínima F1) por cualquier proceso que modifique la consistencia del hígado. Puede observarse valores elevados de la elastrografia, sin que haya fibrosis hepática en pacientes con congestión venosa por falla hepática (ICC), en pacientes con hipertensión biliar secundaria a colestasis extrahepática y en pacientes con hepatitis aguda e incluso crónica agudizada con gran incremento de ALT. Nosotros recomendamos además de una buena historia clínica realizar en Ultrasonido hepatobiliar – pancreático además de tener conocimiento de los niveles de ALT previos al examen y a la vez de la distancia piel cápsula de Glisson ( debe ser menor de 25 mm para sonda M ) antes de realizar e interpretar los resultados. La tasa de fracasos en los que no se obtienen resultados oscila en torno al 4.5 % de las exploraciones realizadas y el principal factor causante es un elevado IMC. Para la sonda M se recomienda pacientes con IMC ojalá no superiores a 30 e idealmente por debajo de 28. El otro factor limitante o de mediciones fallidas son los pacientes con espacios intercostales estrechos.
- Si existe dudas por los antecedentes del paciente o por la dificultad en la técnica pueden apoyarse en otros exámenes que confirmen un grado de fibrosis avanzada con el Fibrotest , APRI, Tac de abdomen e incluso, Dopler y la RMN e incluso la biopsia hepática. Se observo concordancia entre la elastografia y el fibrotest del 70-80 % de los casos y con la biopsia en el 64% de los pacientes con fibrosis significativa, en el 95% de los pacientes con fibrosis avanzada y en el 94% de los pacientes con cirrosis.
- El valor de rigidez óptimo para diagnosticar cirrosis hepática en pacientes con enfermedades colestásicas, NAFLD (Esteatosis hepática ), ingesta de alcohol crónica ó receptores de lóbulo hepático derecho de donante vivo es claramente superior al descrito en pacientes con hepatitis crónica C.
- Otros beneficios del ultrasonido convencional y asociado al doppler previo a la realización de la Elastografia son los hallazgos de signos indirectos de hipertensión portal como la esplenomegalia, la circulación colateral, aumento del diámetro de la vena porta y la disminución de la velocidad del flujo portal ó la aparición de ascitis.
- En algunos casos de patologías con rápido desarrollo de fibrosis como en los pacientes sometidos a trasplante hepático o en otras enfermedades con inflamación hepática aguda o en colestasis extrahepática debe realizarse valoraciones seriadas en el primer caso (3-6,9 y 12 meses ) y en el segundo caso una vez se considera que han disminuidos los niveles de ALT debe repetírsela elastografia para documentar disminución de los resultados iniciales o normalización de los mismos .
La infección crónica por el VHC es a la vez común y un determinante importante de la salud pública en los Estados Unidos. La morbilidad de la infección por VHC es casi completamente relacionada con el desarrollo de la cirrosis. Debido a los Centros para la recomendación de Control de Enfermedades han evaluado a los pacientes nacidos entre 1945 y 1965 para el VHC y la creciente ola de terapias eficaces contra el VHC, debemos anticipar una gran afluencia de pacientes en el orden de 1 millón de personas que buscan atención para el VHC. 1 La elastografia hepática de transición Fibroscan es una excelente opción para estos pacientes, lo que podría resolver el costo y riesgo de la evaluación de la biopsia al tiempo que reduce la vacilación relacionada con el paciente hacia las pruebas de diagnóstico. En consecuencia, es fundamental que los médicos sean capaces de interpretar los resultados de la elastografia hepática fibroscan y conocer sus limitaciones.
«Tradicionalmente, la fibrosis en el VHC ha sido puesta en escena mediante el uso de una variedad de sistemas de puntuación; la 2 más comúnmente utilizados son los puntajes de METAVIR y Ishak. 27 28 Estas puntuaciones fueron diseñados para el estadio de fibrosis a través fibrosis portal, fibrosis en puente, y la cirrosis. Su valor fue más significativo para los ensayos clínicos, lo que ayuda a priorizar los pacientes con fibrosis portal o más avanzado que necesita tratamiento y especialmente en la era del interferón cuando los efectos secundarios del tratamiento limitan la aceptabilidad del paciente, las tasas de respuesta fueron más bajos, y muchos pacientes con enfermedad leve desea aplazar el tratamiento . Ahora, la eficacia de los nuevos tratamientos se aproxima a> 90% respuesta virológica sostenida, y el aumento de la tolerabilidad de los regímenes sin interferón ha hecho que la estadificación exacta de la enfermedad sea menos importante. Por lo tanto para el clínico hoy en día, la estadificación exacta de la enfermedad es menos relevante. Los médicos deben utilizar las nuevas tecnologías para identificar a los pacientes con insuficiencia renal leve o sin fibrosis y, por tanto, las posibilidades de eventos relacionados con el hígado de las personas con enfermedad más avanzada. En este nuevo paradigma, el escenario no debe determinar la elegibilidad tratamiento, pero puede ser utilizado en los países con pocos recursos como el nuestro Colombia para determinar las prioridades para la terapia. El conocimiento más importante derivado de la puesta en escena de la fibrosis en el VHC es la identificación de aquellos pacientes con fibrosis en puente y especialmente cirrosis que deben ser examinados para determinar la presencia de varices esofágicas y del carcinoma hepatocelular. En consecuencia, podríamos considerar la etapa más crítica de la fibrosis en escena como la exclusión de cirrosis con el mayor valor predictivo negativo (VPN).»
Por lo tanto, utilizamos VCTE como la primera prueba crítica de punto de cuidado para excluir la presencia de cirrosis. Descrita por primera vez por Ziol et al 29 en su estudio prospectivo de elastografia hepática FibroScan® comparado con biopsia en 327 pacientes con el VHC, los puntos de corte óptimos para LSM F2 y F4 o mayor (cirrosis) fueron 8,7 y 14,5 kPa, respectivamente. Sin embargo, estudios posteriores han determinado otros puntos de corte. Ese mismo año, Castera et al 24 informó sobre 183 pacientes con VHC consecutivos con valores de corte de 7,1 kPa para ≥F2, 9,5 kPa para ≥F3, y 12,5 kPa para F4. Dos años más tarde, Fraquelli et al 3 identifica los siguientes puntos de corte en una población italiana: 7,9 kPa para ≥F2, 10.3 kPa para ≥F3, y el 11,9 kPa para F4. Arena et al 30 encontró que los pacientes con menos de 12 kPa indican claramente la ausencia de la cirrosis, mientras que un punto de corte de más de 18 kPa indica claramente la cirrosis. Cardoso et al 31 encontraron que el punto de corte de 7,1 kPa tiene un valor de 88% predictivo positivo (VPP) de fibrosis significativa, mientras que el 12,5 kPa tiene un valor presente neto del 98% para la cirrosis. En los Institutos Nacionales de la Salud en su experiencia con VCTE, 7 pacientes con biopsias de falsos negativos y la cirrosis clínica fueron identificados correctamente por un corte de LSM de 13,1 kPa. 32 En nuestras manos, un corte de la rigidez conservadora de 7,3 kPa distingue pacientes estadounidenses sin fibrosis significativa de los que puede con excelente VPN. 7 Recientemente hemos informado de los resultados del estudio de cohorte EE.UU. que incluía nuestra experiencia con más de 900 pacientes estadounidenses con hepatitis viral crónica con un IMC medio de 27,3 kg / m 2. En esta población, los puntos de corte para la fibrosis F3 (puente) fueron 8,5 y 8,6 kPa para los pacientes por encima y por debajo de la mediana del IMC. Los puntos de corte para F4 (cirrosis) fueron 17,1 y 10,4 kPa para los pacientes por encima y por debajo de la mediana del IMC, con la respectiva curva ROC de 0,91 y 0,90. 33
Es importante contextualizar puntos de corte para la fibrosis avanzada por contabilización de las propiedades viscoelásticas de la inflamación crónica. El nivel de ALT se conoce en el momento de elastografia hepática FibroScan® . Se ha sabido por mucho tiempo que la inflamación, aguda y crónica, confunde LSM en pacientes con VHB y poblaciones mixtas de hepatitis viral. 8 34 35 En 2012, se informó en este diario que en un grupo de pacientes con fibrosis F0-F2 confirmado por biopsia, LSM sugerentes de la cirrosis por 3 puntos de corte diferentes 3 24 29 se obtuvieron en pacientes con inflamación histológica de alta calidad, así como en aquellos con ALT alta. Utilizando el punto de corte más conservador, 29 niveles de ALT por encima de 80 y 120 UI / L sugirió un hígado «cirrótico» con OR de 3,84 y 4,10, respectivamente. 7 Estos resultados están apoyados además por la disminución de la rigidez del hígado que los pacientes experimentan durante la terapia antiviral para VHC. 36 37.
La experiencia con VCTE en VHB se ha quedado atrás hasta hace poco de VHC . Desde varios grupos franceses con experiencia VCE conocida llegó algunos de los primeros datos más fuertes. Marcelino et al 38 llevaron a un grupo multicéntrico que evaluó prospectivamente 202 pacientes con biopsia emparejado y LSM. El porcentaje fue de 0,81 y 0,93 para ≥F2 y F4. Sus valores de corte óptimo LSM fueron 7,2 y 11,0 kPa para ≥F2 y F4, respectivamente. Mediante el uso de puntos de corte de 11,0 y 18,2 kPa, los respectivos VPP / VPN para la cirrosis fueron del 38% / 99% frente a 67% / 96%. El rendimiento de estos puntos de corte se ha confirmado en manos de otros. 31 Un reciente meta-análisis de estudios publicados que comprenden a 2772 pacientes, se evaluó el rendimiento de la elastografia hepática Fibroscan en VHB crónica. Catorce de los 18 estudios incluidos en este análisis eran estrictamente VHB exclusiva. Los puntos de corte para la F2 (o mayor), F3-F4 y F4 fueron 7,9 kPa, 8,8 kPa y 11,7 kPa, respectivamente. Un LSM de 11,7 kPa tuvo una sensibilidad del 84,6% y una especificidad del 81,5% para la detección de la cirrosis.
Tanto en HBV como en HCV, existe la posibilidad de un aumento de falsos positivos en la rigidez hepática medida como resultado de la actividad necroinflamatoria. 40 Una de las primeras señales de que la inflamación crónica, reflejada por el nivel de ALT, afectado fiabilidad de la Elastografía hepática Fibroscan en VHB provino del estudio de Oliveri et al 8 de 297 pacientes italianos consecutivos con VHB crónica. Entre los pacientes con fibrosis etapa idéntica, aquellos con niveles elevados de ALT tuvieron mayor LSM. LSM también aumentó 1,3 veces a 3 veces durante los brotes de VHB detectado durante la evaluación. Este hallazgo es más fácilmente reproducibles, totalmente inadecuada en un grupo de 12 pacientes cirróticos con VHB aguda. 6 9 41 Nueve de sus pacientes (75%) tenían LSM mayor que 11,9 kPa en la presentación, lo que sugiere la cirrosis. En la semana 24 después de la resolución de la hepatitis aguda, ninguno tenía LSM superior a 11,9 kPa. 41 Para determinar la contribución relativa a la rigidez del hígado de cada nivel de actividad viral, Fung et al 42 evaluaron prospectivamente 157 pacientes en Hong Kong. VCTE se realizó en sujetos sanos, así como en aquellos con HBV oculta (la carga viral positiva, antígeno de superficie negativa), HBV activo (antígeno de superficie positivo y la carga viral), y HBV-cirrosis. Los LSM respectivas de estos grupos fueron 4,6 kPa (2,0 a 7,1), 4,2 kPa (3.4 a 6.9), 8.7 kPa (3,6 a 44,3) y 33,8 kPa (11,9-75). Claramente, ALT puede confundir PPV de VCTE y debe considerarse al interpretar sus resultados.
Debido a las directrices explícitamente se basan las recomendaciones de tratamiento del VHB en la inflamación (ALT), la carga viral, y con frecuencia la histología, el efecto de confusión de la ALT tiene una dimensión añadida de importancia. De acuerdo con ello, Chan et al 43 sugieren un algoritmo basado en ALT para el uso de VCTE en HBV. Sobre la base de su experiencia con 161 pacientes chinos sometidos VCTE emparejado y biopsia, este grupo sugiere que cuando los pacientes tienen una puntuación normal ALT por encima o por debajo de los puntos de corte VCTE para la fibrosis significativa (en su estudio 5 kPa o menos frente a 9,0 kPa o mayor), uno puede tomar decisiones de tratamiento sin una biopsia de hígado, reservando la biopsia de pacientes con resultados indeterminados (por ejemplo, 6-9 kPa). Sin embargo, para los pacientes con ALT elevada (mayor que el límite superior de lo normal), se utilizó la biopsia hepática en una zona indeterminada expandida de 7 a 12 kPa. 43 En la práctica clínica, se podría sustituir la biopsia para la evaluación serológica de la fibrosis (Figura 2).
El Hígado graso no alcohólico es prevalente en el 46% de los estadounidenses y la esteatohepatitis no alcohólica (NASH) en más de un 12%, y las tasas están aumentando de manera significativa a nivel mundial. 44 45 Debido al tamaño de la población con hígado graso no alcohólico, existen preocupaciones legítimas de salud pública en relación con el costo y riesgo de la evaluación de la biopsia para la enfermedad avanzada. La biopsia se utiliza para el estadio de fibrosis y para diferenciar la esteatosis simple a partir de NASH, y nuevos sistemas de puntuación propuesto para diagnosticar NASH se basan en la esteatosis, la inflamación y apoptosis. 46 Dado que el APV no puede diferenciar de forma fiable las características histológicas de la EHNA, debe tenerse en cuenta que el APV sólo se puede utilizar para determinar el grado de fibrosis o presencia de cirrosis y no a diagnosticar o descartar la EHNA. 47 Los principales problemas que afectan a la Elastografia hepática Fibroscan en hígado graso no alcohólico son un aumento en los exámenes fallidos o sesgados debido a índice de masa corporal elevados o potencialmente debido a la confusión por la esteatosis. 44 La razón más común para el fracaso de VCTE es un índice de masa corporal mayor de 30 kg / m 2, en donde la tasa de fracaso es informado de 22% -25%. 48 49
El efecto de la esteatosis en la rigidez del hígado es controvertida, pero varios estudios han explorado esta relación. Por ejemplo, Gaia et al 50 encontró que los pacientes con NAFLD con F3 y esteatosis severa tenían valores de LSM inferiores, similares a los de los pacientes con F1 y esteatosis leve. Mediante el uso de un corte de 8 kPa, la elastografia hepática Fibroscan subestimó el estadio de fibrosis en el 75% de los pacientes con esteatosis F3 y severa. Sin embargo, mediante el uso de un corte similar de 8,75 kPa para ≥F3 la fibrosis, Petta et al 51 encontraron una tasa de falsos negativos del 24%. En el estudio más grande, Wong et al 48 estudiaron prospectivamente 246 pacientes consecutivos a partir de centros en China y Francia, y mediante el uso de un corte de 10,3 kPa, se encontraron con un 99% y un 46% VAN PPV para el diagnóstico de la cirrosis.
La llamada sonda XL fue diseñado para superar la adiposidad de la pared torácica y mejorar las características de prueba de la elastografia hepática en una población obesa. Hay evidencia de que su funcionamiento es reproducible. En comparación con la sonda M, la sonda XL tiene un diámetro mayor en la punta, menor frecuencia central, y una mayor amplitud de vibración. Críticamente, se evalúa la rigidez del hígado a mayor profundidad (3.5-7.5 cm). Los pacientes obesos pueden experimentar tasas similares de de éxito de LSM cuando se utiliza esta sonda modificada. 52 53 54 55 Por ejemplo, Myers et al 54 han demostrado en una población de 276 pacientes con enfermedad hepática crónica y el IMC> 28 kg / m 2, que la tasa de fracaso fue significativamente menor con la sonda XL que con la sonda M (1,1% frente al 16%; p <0,00005). Sin embargo, siguen siendo cuestionables 2. En primer lugar, incluso con la sonda XL, aunque en menor grado que la sonda M, la fiabilidad de Elastografia hepática de transicion disminuye para los pacientes con un IMC mayor de 30 kg / m 2. 53 Asimismo, los resultados poco fiables aún se observan con la sonda XL en 25% de los casos en comparación con el 50% de los casos con la sonda M (p <0,00005). 54 En efecto, la sonda XL y la histología son discordantes en hasta el 9% de los pacientes con un IMC mayor de 35 kg / m 2. 49 En segundo lugar, la sonda XL puede generar LSM más baja que la sonda anterior M en el mismo paciente, lo que sugiere que los puntos de corte de fibrosis específicos de la enfermedad pueden necesitar ser más baja en los exámenes de sonda XL. Múltiples investigadores han encontrado que LSM por la sonda XL es menor que por la sonda M por tanto como 1,7 + 2,3 kPa. 49 54 Por lo tanto, aunque estas nuevas sondas mejorar la fiabilidad de VCTE en pacientes obesos, se necesita más investigación para determinar el IMC puntos de corte para la confiabilidad y precisión.
Enfermedad hepática alcohólica y Elastografia hepática fibroScan
Especialmente en sus primeras etapas, la enfermedad hepática alcohólica se caracteriza por fibrosis sinusoidal, la esteatosis y la inflamación significativa; por lo tanto, por LSM VCTE es susceptible a los factores de confusión. La abstinencia puede afectar dramáticamente los resultados VCTE. Reproducible, la abstinencia se asocia con una disminución más o menos 4,9 kPa en LSM. 56 57 58 redujo significativamente LSM se puede ver incluso después de 7 días de abstinencia. LSM disminuyó desde 7,2 hasta 6,1 kPa en 7 días de sobriedad en un estudio, lo que resulta en una reducción en la etapa de fibrosis estimado en 32 pacientes (23,3%). 59 Nahon et al 60 examinó el papel de VCTE en una población francesa de 147 pacientes con enfermedad hepática alcohólica que se someten emparejados LSM y la biopsia, el 53,7% de los cuales tenía cirrosis y el 28,7% de los cuales tenían moderada a marcada hepatitis alcohólica en la biopsia. Mediante el uso de puntos de corte óptimos de 12,96 y 22,7 kPa, las AUROCs eran 0,94 y 0,87 para el diagnóstico de fibrosis avanzada y cirrosis, respectivamente. Con exclusión de los pacientes que estaban tomando activamente, Mueller et al 57 encontró que un corte de 12,5 kPa tenía una curva ROC de 0,91 para la fibrosis F4. Por lo tanto, cuando se utiliza la elastografia hepática Fibroscan para evaluar pacientes con enfermedad hepática alcohólica, el médico debe tener en cuenta tanto los hábitos de consumo actuales y la presencia de la esteatohepatitis alcohólica activa. Se recomienda 7 días de abstinencia al alcohol y una ALT por debajo de 100 ui/dl
PROPUESTA DE ALIANZA - Servicio de FibroScan
PRECIO OFERTADO POR EXAMEN POR PACIENTE :
$840.000.00 ( Ochoscientos cuarenta mil pesos )
- Requisitos fuera de Bogotá para garantizar volumen mínimo de 20 pacientes ( 3 horas y 20 minutos )
- Tiempo por paciente disponer de 10 minutos ( 6 pacientes por hora )
- % para quien coloca los pacientes 30% sin colocar viáticos de traslados, gastos de calibración ni de estadía o depreciación ( 20 millones de pesos por año ) y 50% en caso de cubrir la mitad de todo ingresos y egresos
Atte
DR GUILLERMO PEREZ GONZALEZ Md
Internista – Gastroenterólogo Certificado En Elasografia hepaTICA Echosens Francia
RM 92550185
- Pinzani M, Vizzutti F, Arena U, Marra F. Technology insight: Non invasive assessment of liver fibrosis by biochemical scores and elastography. Nat Clin Pract Gastroenterol Hepatol. 2008;5:95-106.
- Fontana RJ, Goodman ZD, Dienstag JL, Bonkovsky HL, Naishadham D, Sterling RK, et al. Relationship of serum fibrosis markers with liver fibrosis stage and collagen content in patients with advanced chronic hepatitis C. Hepatology. 2008;47:789-798
- Poynard T, Morra R, Halfon P, Castera L, Ratziu V, Imbert-Bismut F, et al. Meta-analyses of Fibrotest diagnostic value in chronic liver disease. BMC Gastroenterol. 2007;7:40-40.
- Rosenberg WM, Voelker M, Thiel R, Becka M, Burt A, Schuppan D, et al. Serum markers detect the presence of liver fibrosis: A cohort study. Gastroenterology. 2004;127:1704-1713.
- Aguirre DA, Behling CA, Alpert E, Hassanein TI, Sirlin C.B. Liver fibrosis: Non invasive diagnosis with double contrast material-enhanced MR imaging. Radiology. 2006;239:425-437.
- Colli A, Fraquelli M, Andreoletti M, Marino B, Zuccoli E, Conte D. Severe liver fibrosis or cirrhosis: Accuracy of US for detection–analysis of 300 cases. Radiology. 2003;227:89-94.
- Romero-Gómez M, Gómez-González E, Madrazo A, Vera-Valencia M, Rodrigo L, Pérez-Álvarez R, et al. Optical analysis of computed tomography images of the liver predicts fibrosis stage and distribution in chronic hepatitis C. Hepatology. 2008;47:810-816.
- Castera L, Vergniol J, Foucher J, Le Bail B, Chanteloup E, Haaser M, et al. Prospective comparison of transient elastography, Fibrotest, APRI, and liver biopsy for the assessment of fibrosis in chronic hepatitis C. Gastroenterology. 2005;128:343-350.
- Angulo P. Nonalcoholic fatty liver disease. N Engl J Med. 2002;346:1221-1231.
- Yoneda M, Yoneda M, Mawatari H, Fujita K, Endo H, Iida H, et al. Noninvasive assessment of liver fibrosis by measurement of stiffness in patients with nonalcoholic fatty liver disease (NAFLD). Dig Liver Dis. 2008;40:371-378.
- Foucher J, Chanteloup E, Vergniol J, Castera L, Le Bail B, Adhoute X, et al. Diagnosis of cirrhosis by transient elastography (Fibroscan): A prospective study. Gut. 2006;55:403-408
- Nahon P, Kettaneh A, Tengher-Barna I, Ziol M, De Lédinghen V, Douvin C, et al. Assessment of liver fibrosis using transient elastography in patients with alcoholic liver disease. J Hepatol. 2008;49:1062-1068.
- Pungpapong S, Nunes DP, Krishna M, Nakhleh R, Chambers K, Ghabril M, et al. Serum fibrosis markers can predict rapid fibrosis progression after liver transplantation for hepatitis C. Liver Transpl.2008;14:1294-1302.
- Utilidad del Fibroscan para evaluar la Fibrosis hepática. José A Carrión . Instituto De Investigaciones Biomédicas (IDIBAPS) CIBER de enfermedades hepáticas y digestivas . HospitalClinic.Barcelona.España
- Tapper E.B., Cohen E.B., Patel K., et al: Levels of alanine aminotransferase confound use of transient elastography to diagnose fibrosis in patients with chronic hepatitis C virus infection. Clin Gastroenterol Hepatol 2012; 10: pp. 932-937
- Oliveri F., Coco B., Ciccorossi P., et al: Liver stiffness in the hepatitis B virus carrier: a non-invasive marker of liver disease influenced by the pattern of transaminases. World J Gastroenterol 2008; 14: pp. 6154-6162
- Castéra L., Foucher J., Bernard P.H., et al: Pitfalls of liver stiffness measurement: a 5-year prospective study of 13,369 examinations. Hepatology 2010; 51: pp. 828-835
- Arena U., Vizzutti F., Corti G., et al: Acute viral hepatitis increases liver stiffness values measured by transient elastography. Hepatology 2008; 47: pp. 380-384 Arena U.,
- Lupsor Platon M., Stasi C., et al: Liver stiffness is influenced by a standardized meal in patients with chronic HCV hepatitis at different stages of fibrotic evolution. Hepatology 2013; 58: pp. 65-72
- Mederacke I., Wursthorn K., Kirschner J., et al: Food intake increases liver stiffness in patients with chronic or resolved hepatitis C virus infection. Liver Int 2009; 29: pp. 1500-1506
- Friedrich-Rust M., Ong M.F., Martens S., et al: Performance of transient elastography for the staging of liver fibrosis: a meta-analysis. Gastroenterology 2008; 134: pp. 960-974
- Castéra L., Vergniol J., Foucher J., et al: Prospective comparison of transient elastography, Fibrotest, APRI, and liver biopsy for the assessment of fibrosis in chronic hepatitis C. Gastroenterology 2005; 128: pp. 343-350
- Castera L.: Noninvasive methods to assess liver disease in patients with hepatitis B or C. Gastroenterology 2012; 142: pp. 1293-1302
- Gara N., Zhao X., Kleiner D.E., et al: Discordance among transient elastography, aspartate aminotransferase to platelet ratio index, and histologic assessments of liver fibrosis in patients with chronic hepatitis C. Clin Gastroenterol Hepatol 2013; 11: pp. 303-308
- Afdhal N.H., Bacon B.R., Patel K., et al: Diagnosis accuracy of liver stiffness (FibroScan®) in patients with chronic viral hepatitis: results of a large USA cohort. Hepatology 2013; 58: pp. 278A-279A
- Coco B., Oliveri F., Maina A.M., et al: Transient elastography: a new surrogate marker of liver fibrosis influenced by major changes of transaminases. J Viral Hepat 2007; 14: pp. 360-369
- Verignol J., Foucher J., Castéra L., et al: Changes of non-invasive markers and FibroScan values during HCV treatment. J Viral Hepat 2009; 16: pp. 132-140
- Viganò M., Massironi S., Lampertico P., et al: Transient elastography assessment of the liver stiffness dynamics during acute hepatitis B. Eur J Gastroenterol Hepatol 2010; 22: pp. 180-184
- Fung J., Lai C.L., Chan S.C., et al: Correlation of liver stiffness and histological features in healthy persons and in patients with occult hepatitis B, chronic active hepatitis B, or hepatitis B cirrhosis. Am J Gastroenterol 2010; 105: pp. 1116-1122
- Chan H.L., Wong G.L., Choi P.C., et al: Alanine aminotransferase-based algorithms of liver stiffness measurement by transient elastography (Fibroscan) for liver fibrosis in chronic hepatitis B. J Viral Hepat 2009; 16: pp. 36-44
- Festi D., Schiumerini R., Marzi L., et al: Review article: the diagnosis of non-alcoholic fatty liver disease—availability and accuracy of non-invasive methods. Aliment Pharmacol Ther 2013; 37: pp. 392-400
- Chalasani N., Younossi Z., Lavine J.E., et al: The diagnosis and management of non-alcoholic fatty liver disease: practice guideline by the American Association for the Study of Liver Diseases, American College of Gastroenterology, and the American Gastroenterological Association. Hepatology 2012; 55: pp. 2005-2023
- Kleiner D.E., and Brunt E.M.: Nonalcoholic fatty liver disease: pathologic patterns and biopsy evaluation in clinical research. Semin Liver Dis 2012; 32: pp. 3-13
- Castera L., Vilgrain V., and Angulo P.: Non invasive evalutation of NAFLD. Nat Rev Gastroenterol Hepatol 2013; 10: pp. 666-675
- Wong V.W., Vergniol J., Wong G.L., et al: Diagnosis of fibrosis and cirrhosis using liver stiffness measurement in nonalcoholic fatty liver disease. Hepatology 2010; 51: pp. 454-462
- Wong V.W., Vergniol J., Wong G.L., et al: Liver stiffness measurement using XL probe in patients with nonalcoholic fatty liver disease. Am J Gastroenterol 2012; 107: pp. 1862-1871
- Gaia S., Carenzi S., Barilli A.L., et al: Reliability of transient elastography for the detection of fibrosis in non-alcoholic fatty liver disease and chronic viral hepatitis. J Hepatol 2011; 54: pp. 64-71