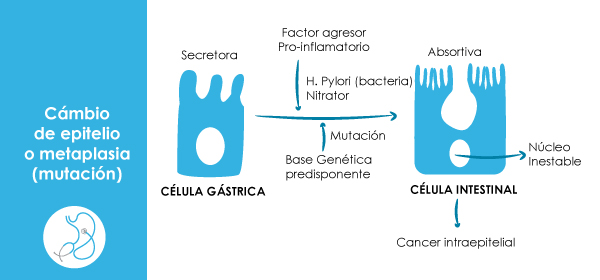
CANCER GASTRICO METAPLASIA GASTRICA Y ATROFIA ?
La detección temprana del cáncer gástrico asociada a metaplasia gástrica intestinal y atrofia es posible .La incidencia del cáncer gástrico sigue siendo elevada en las regiones montañosas de Colombia como en Bogotá y en especial en Nariño. Por lo anterior asociado a los avances en las técnicas de detección temprana del cáncer gástrico por endoscopia cada día se detectan más lesiones precancerosas y canceres del estomago en estadios iniciales aumentando as las tasa de curabilidad lo cual se ven en los controles de la consulta de seguimiento de gastroenterología .El descubrir que el cáncer gástrico es causado por la infección de una bacteria el Helicobacter pylori (h. pylori ) convirtió su erradicación en la principal estrategia de prevención. Con pocas excepciones el hallar H. pylori en un paciente (provoca daño de los tejidos e inestabilidad genética), debe ser tratado para disminuir el riesgo de padecer adenocarcinoma gástrico (AG); no obstante esta estrategia no elimina el riesgo total de padecerlo.
Existen 2 tipos de cáncer gástrico referente al más común el adenocarcinoma de tipo intestinal (80%); éste tipo posee un fondo medio ambiental mayor y esta asociada a la secuencia inflamación (gastritis), metaplasia, displasia, atrofia y cáncer . El otro tipo o adenocarcinoma difuso (20%) éste último por lo general es de células en anillo de sello se detecta a edades más tempranas y tiene mayor fondo genético familiar.
La progresión paso a paso desde la mucosa gástrica normal a cáncer del estomago fue descrita por el médico colombiano Pelayo Correa quien incluyo a la metaplasia intestinal como un precursor del cáncer gástrico ( En 1975 era mucosa normal , gastritis superficial, metaplasia intestinal delgada, metaplasia colonica, displasia leve , displasia severa , carcinoma gástrico y finalmente cáncer invasor; lego en 1992: mucosa normal., gastritis superficial, gastritis atrófica, metaplasia de intestino delgado (completa), metaplasia colonica ( incompleta ) y cáncer gástrico ) . El riesgo de desarrollar cáncer gástrico es mayor se coexisten la metaplasia gástrico intestinal incompleta (intestino delgado) y la atrofia gástrica.
El estomago puede ser dividido en 2(dos) regiones con características de tejido (histológicas), apariencia, localización y funciones diferentes:
- La mucosa del cuerpo gástrico (mucosa oxintica, con pliegues gruesos con foveolas en la cual existe un epitelio columnas secretor de moco y células parietales responsables de la secreción de acido, células enterocromafines que secretan histamina y células que secretan pepsina además de factor intrínseco). Esta mucosa gradualmente se transforma en
- La mucosa antral (distal) las glándulas son principalmente tubulares secretoras de moco con células endocrinas (células G que secretan gastrina y células D que secretan somatostatina) lo cual juegan un papel importante en la secreción de acido.
La región más proximal a las anteriores es el cardias, es corta mide aprox. 2 cm, es un segmento tubular corto vecino a la mucosa esofágica entre esta y la mucosa oxintica.
El epitelio gástrico es resistente al acido y a los jugos digestivos y rápidamente repara un daño causado por sustancias químicas como los AINES (anti-inflamatorios no esteroideos), las biopsias o cualquier inflamación. El proceso reparativo es similar al visto en el intestino, excepto por la localización del sitio de proliferación, el cual en el cuerpo del estómago es en el cuello glandular regenerando mucosa que asume el fenotipo del epitelio pilórico (mucoprotector ) y expresa el factor trébol II ( TFF2 o péptido espasmolítico en animales SPEM ). La nueva mucosa gástrica, en humanos es llamada mucosa pseudopilorica, metaplasia mucosa, o metaplasia pilórica, simula la mucosa antral y es considerada como un confiable marcador de reparación de la mucosa oxintica. La profundidad, cronicidad y extensión del daño/inflamación asociada con metaplasia pseudopilorica determina si las progresiones posteriores a transformación metaplasica que expresen células globo similares a las observadas en el intestino inician la metaplasia intestinal. Aunque este proceso de reparación y restauración de la mucosa oxintica puede llegar a feliz término pueden quedar áreas focales o parches de mucosa metaplasica residual que persisten indefinidamente; estos parche (no contiene mucosa gástrica nativa) constituyen tanto en forma y función la expresión de la atrofia gástrica.
Tanto en estudios experimentales como observacionales se ha determinado que la mucosa gástrica metaplasica es reversible y puede no progresar directamente a cáncer gástrico. A menos que Ocurra un biomarcador antes de la injuria gástrica y reparación. El riesgo de cáncer gástrico está asociado con la severidad, extensión y con mayor grado con la causa de los cambios atróficos. En casos específicos se puede señalar un riesgo incrementado para el desarrollo del epitelio (adenocarcinoma) o tumor neuroendocrino (carcinoide).
La presencia de metaplasia intestinal en una muestra de biopsia de mucosa gástrica realizada durante una endoscopia da pie para indagar si fue un pequeño remanente de un daño previo que siguió a un proceso de reparación, no obstante puede ser algo insignificante o el presagio de posibles daños. Debe realizarse una valoración estratificada del riesgo futuro individual de desarrollar cáncer gástrico.
La atrofia gástrica es definida con un tipo de pérdida de las glándulas nativas y tiene 2 causas principales: la infección con H pylori y la autoinmunidad. Cado uno de ellas presenta una distribución topográfica distinta de atrofia y predisponen a diferentes tumores gástricos.
El H pylori causa inflamación, daño celular progresivo e inestabilidad genética que inicia en el antro gástrico y progresa después al cuerpo. En el antro esta bacteria interactúa con las células de la superficie y con las foveolares. En el cuerpo debido a la alta concentración de ácido producida por las células oxintica lo cual dificulta la adherencia de h pylori a la superficie celular. No obstante cuando ocurre un daño en la producción de ácido como ocurre cuando existe fiebre, malnutrición, ingesta de medicamentos antiácidos puede alterar este balance. En condiciones normales, el H pylori induce inflamación, daño de la mucosa extendiéndose desde el antro hasta el cuerpo debido a la progresión de la inflamación. Al extenderse proximalmente provoca atrofia de la mucosa corporal en la cual las células principales y las parietales son escasas o ausentes (metaplasia pseudopilorica). La distancia entre la incisura angularis y la unión gastroesofágica es más corta en la curva menor que en la mayor y esto puede explicar en parte el por qué el proceso de atrofia avanza más rápidamente de esta manera. La incisura angularis es por lo general el primer sitio donde aparece la atrofia y es el blanco del lugar donde se toman las biopsias en el sistema de clasificación de Sydney.
En la gastritis autoinmune, la lesión esencial es una infiltración linfocítica destructiva de la mucosa oxintica; con el tiempo desparecen las células oxinticas y son reemplazadas por células productoras de moco, cuando la enfermedad progresa el cuerpo gástrico es reemplazado por grandes áreas de metaplasia intestinal y pseudopilorica. El resultado de la hipoclorhidria induce hiperplasia y en algunos casos displasia de las células parecidas a las enterocromafines. En la ausencia de infección concomitante con H pylori, la gastritis autoinmune es estrictamente limitada al cuerpo. La mucosa antral por lo general presenta una apariencia reactiva con solamente leve incremento de la inflamación crónica.
¿Cómo se reconoce la gastritis atrófica?
Se define como pérdida de las glándulas nativas con desaparición de las unidades glandulares o con transformación metaplasica (metaplasia pseudopilorica e intestinal) de las glándulas nativas. Lo común es que coexista metaplasia intestinal con atrofia. En el antro la fibrosis de la lámina propia en particular cuando esta separa las partes más profundas de las colas glandulares desde la muscular propia es típico de atrofia; puede haber denso infiltrado inflamatorio lo cual minimiza las pérdidas glandulares.
¿ Que hacer se detecta la metaplasia gástrica intestinal ?
- Localización ( antro , cuerpo o ambas )
- Extensión: Local o difusa?
- Tipo ( atrofia no metaplasica, metaplasia pseudopilorica y metaplasia intestinal?
- Causas: H. pylori, autoinmune, daño tóxico etc.
- Puntuación de estratificación de riesgo ( endoscópica e histológica )
Tres tipos de pacientes que pueden presentar metaplasia/atrofia y ó daño tisular:
a. Daño focal dado por gastritis y úlceras inducida por la ingesta de AINES; las cuales pueden ser reparadas por escaras dentro de la mucosa de apariencia normal.; no obstante la mucosa puede mostrar focos de metaplasia intestinal reportado en el informe pero esta no es significativa.
b. Un paciente con gastritis por H. pylori, con múltiples focos o grandes zonas de metaplasia intestinal en las muestras de biopsias del antro y del cuerpo indican que padecen un proceso destructivo que conlleva a un riesgo incrementado de cáncer gástrico.
c. La metaplasia intestinal limitada al cuerpo con mucosa antral normal debe investigarse gastritis autoinmune la cual tienen un riesgo bajo de adenocarcinoma pero una alta probabilidad de proliferación neuroendocrina.
Utilidad y técnica adecuada de toma de biopsias gástricas: La endoscopia en Bogotá, es un procedimiento invasivo de bajo riesgo; los endoscopios modernos con magnificación e imágenes de banda estrecha (NBI) pueden identificar mejor las anormalidades de la mucosa para así dirigir las biopsias. Un inconveniente es el método de tomar biopsias al azar y el patólogo no puede saber de dónde se tomaron las biopsias y su significado. Aunque lo anterior no es importante si es normal; pero es importante en caso de encontrar atrofia ya debe localizarse con la mayor exactitud posible para obtener los suficientes datos para evitar nuevas biopsias.
En la metaplasia pseudopilorica en cual las biopsias del cuerpo histológicamente se parecen a las del antro, idealmente el patólogo debe utilizar una coloración ideal tal como el pepsinógeno I ó para TFF2 ó péptido espasmolítico.
RECOMENDACIONES EN LA TOMA DE BIOPSIAS GASTRICAS
Cuando se toman biopsias del estómago no importa el motivo se debe aportan suficiente información al patólogo acerca del estado de la mucosa. Un ejemplo la biopsias de una lesión focal de aspecto normal se toma de sus bordes lo cual facilita definir la causa de la lesión.
La valoración de la totalidad de la mucosa gástrica lo mejor es utilizar el protocolo de biopsias del Sistema Sydney el cual consiste en tres (3) biopsias del antro: curvatura mayor (1) curvatura menos (1) a nivel de la mitad del antro e incisura angularis (1) y dos (2) del cuerpo a nivel de la mitad de la curvatura mayor (1) y menor (1). Las biopsias del antro y cuerpo deben ser colocadas en frascos separados ya que la metaplasia pseudopilorica corporal puede confundirse con la antral y puede confundir a patólogos menos experimentados. El set de biopsias gástricas no debe mezclarse con las biopsias dirigidas a lesiones focales.
Siempre debe incluirse en la solicitud del estudio del tejido a los patólogos:
- Sitio de toma de la biopsia
- Por qué fueron tomadas
- Que se vio endoscópicamente
- Que resultado se espera
Recomendaciones adicionales al tomar biopsias gástricas:
- Usar pinzas Jumbo ( la más grande que quepa en el canal )
- No mezclar biopsias de mucosa de aspecto normal con la de lesiones focales de aspecto patológico
- No mezclar biopsias del antro con las del cuerpo
- Tomar un adecuado número de biopsias
- Colocar máximo 5 biopsias por frasco
- Identificar y separar las biopsias según las diferentes tipos de lesiones
- Si la mucosa presenta un gastritis o lesión difusa utilizar el Sistema Sydney
- Tomar fotos de buena calidad de las lesiones biopsiadas
- Optar su opinión diagnóstica o diagnóstico endoscópico
INTERPRETACION CLINICA DE LA METAPLASIA INTESTINAL Y EXPLICACION DESDE UN REPORTE DE PATOLOGIA DE MUESTRAS GASTRICAS TOMADAS POR ENDOSCOPIA
La presencia de metaplasia intestinal solamente significa que un daño en la mucosa gástrica a ocurrido y que ha sido reparado pero sin volver a su estado previa al daño. Pero la pregunta es si ése daño fue un solo evento aislado o es parte de un proceso crónico. Para esto es importante definir juntos con el clínico y el patólogo su localización y extensión teniendo en cuenta el % de muestras que presentan metaplasia. En los países occidentales para valorar el riesgo de cáncer gástrico se utiliza el sistema de valoración gástrica de la atrofia gástrica (OLGA) o la valoración gástrica de la metaplasia intestinal ( OLGUIN).
El sistema o estadiage OLGA está basado sobre una combinación de puntuación de atrofia, es obtenido con muestras de biopsias de las mucosas oxintica y antral( protocolo sistema Sydney) La combinación de estas puntuaciones expresadas en etapas, representa una medida semicuantitativa de la severidad de la enfermedad, el cual va en paralelo al riesgo de malignidad ( OLGA etapas 0- I- II: de muy bajo a bajo riesgo de cáncer ; OLGA etapas III-IV: alto riesgo de cáncer gástrico ) .Estudios prospectivos han determinado de que el sistema OLGA da valor pronóstico para estadificar la gastritis y es aplicable a la práctica clínica.
Bibliografía:
1. Correa P, et al A model for gastric cancer epidemiology. Lancet 1975: 2-58-60
2. Correa P Human gastric carcinogenesis: a multistep and multifactorial process- First American Cancer Society Award Lecture on Cancer Epidemiology and Prevention. Cancer Res 1992: 52: 6735-6740
3. Rugge M, Correa P, et al . Gastric mucosal atrophy : interobserver consistency using new criteria for classificationand grading. Aliment Pharmacol Ther 2002;16:1249-1259.
4. Rugge M , Et al . Gastritic staging in the endoscopic follow-up for the secondary prevention of gastric cancer : a 5 – year prospective study of 1755 patients . Gut 2019;68:11 – 17.
5. Dixon MF, Genta RM , Yardley JH, Correa P , et al Clasification and grading of gastritis. The update Sydney System internationalWorkshop on theHistopatol of gastritis, Houston 1994. Am J Surg Pathol 1996;20:1161-1181.
6. Tan MC, El al . Gastric cancer worldwide except Japan. In:Japan – Singapure. Springer; 2018 pp. 17-28
7. Graham DY. Helicobacter pylori update: gastric cancer, reliable theraphy,and possiblebeneficts. Gastroenterology2015:148:719.e3-731.e3.
8. Sugano K Et al. Kyoto global Consensus report on Helicobacter pylori gastritis .Gut 2015:64:1353-1367.
9. El Serag HB, Et al .Houston Consensus Conference on testing for Helicobacter pylori infection in EEUU. Clin Gastroenterol Hepatol 2018 ; 16:992-1002.
10.David Y Graham, Massimo Rugge , and Robert M Genta. Diagnosis: gastric intestinal metaplasia- what to do next ?Current Opinion Review.Pag 535-545
DR GUILLERMO SEGUNDO PEREZ GONZALEZ . Médico Internita Gastroenterólogo. Bogotá.
Leave a reply
Leave a reply