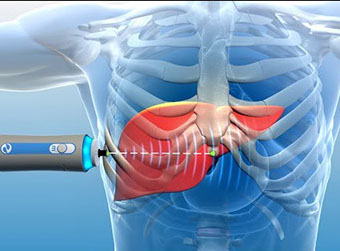
FibroScan o Elastografía o Elastosonografia hepática
La Elastografia hepática de Transición FibroScan o Elastosonografia en Bogotá es el examen de lección para la estadificación de la fibrosis hepática y de la Cirrosis sin someterse a los riesgos de la Biopsia hepática.
FibroScan es una tecnología única no invasiva para cuantificar los diferentes grados de fibrosis o cirrosis hepática sin riesgo que permite vigilar la respuesta al tratamiento valorando 100 veces más tejido hepático que la biopsia del hígado . Aporta una alta probabilidad diagnóstica sobre todo en estadios avanzados y se correlaciona con la escla Metavir de los estudios al microscopia del tejido hepático.
Con la revisión generalizada y tratamientos cada vez más eficaces para los pacientes con hepatitis viral, así como el aumento de la prevalencia de la enfermedad de hígado graso no alcohólico ó esteatosis hepática , la población que es tratada por los gastroenterólogos y hepatólogos es seguro que aumentará. La valoración de la enfermedad hepática avanzada es tradicionalmente invasiva y costosa. La elastografía hepática de transición controlada (VCTE), comúnmente administrada por el dispositivo FibroScan, es una opción aprobado en Europa hace más de una década y hace un año por la Administración de Alimentos y Medicamentos (FDA) de EEUU, para la evaluación no invasiva de la enfermedad hepática en el punto de atención.
A que pacientes deben realizarse la Elastografia hepática FibroScan:
- Hepatitis C Crónica pre tratamiento y post de seguimiento
- Hepatitis C crónica diagmóstico y seguimiento
- Higado graso no alcohólico
- Higado Graso Alcohólico
- Obesidad
- Diabetes
- Dislipidemia ( Elevacion de colesterol o trigliceridos)
- Hiperuricemia ( elevación de ácido úrico )
- Elevación de aminotransferasas ( en especial ALT )
- Enfermedad hepática crónica por Alcohol
- Chequo de Rutina hacia los 40 años de edad
- Antecedentes familiares de hemocromatosis
En Europa desde su introducción hace 10 años en Francia, este examense ha convertido rápidamente en muy popular no sólo entre los pacientes, sino también entre los médicos como una técnica de punto de atención que se podrían utilizar en la consulta externa. En consecuencia, el uso elastografia hepática fibroscan traduce en una disminución significativa en la necesidad de una biopsia hepática para el tratamiento de los pacientes con hepatitis C en la práctica habitual, y esta tendencia ya se ha observado en la mayoría de los países donde se ha implementado elastografia hepática fibroscan . La elastografia hepática fibroscan es ahora ampliamente utilizado en Europa y ha sido adoptado como herramienta de primera línea para la evaluación de la fibrosis hepática en pacientes sin tratamiento previo con hepatitis C sin comorbilidades en Francia después de una revisión sistemática independiente por parte de las autoridades sanitarias francesas
Como la fibrosis hepática progresa a cirrosis, hipertensión portal, y sus complicaciones concomitantes, hay un aumento significativo de la morbilidad y la mortalidad. Los elementos clave en el diagnóstico de la fibrosis y estratificación del riesgo a partir de entonces confían en las herramientas invasivos como la biopsia de hígado a la etapa de la fibrosis y la endoscopia para la detección de las varices. Estas pruebas son costosos y están asociados con riesgo. Además, en el contexto de la revisión generalizada para la hepatitis C (VHC) y de la hepatitis B (VHB) y tratamientos cada vez más eficaces para los pacientes con hepatitis viral, así como el aumento de la prevalencia de la enfermedad de hígado graso no alcohólico (NAFLD), la población que está al cuidado de médicos especialistas del hígado seguramente aumentará. 1 Ahora más que nunca, hay una necesidad crítica de una herramienta no invasiva, segura, rápida, barata y fiable para evaluar a estos pacientes en el punto de atención.
La elastografía hepática de transición Fibroscan es un ecógrafo u ultrasonografo comúnmente administrada por el dispositivo FibroScan (Echosens, París, Francia) es una opción recientemente aprobado por la Administración de Drogas y Alimentos (FDA) para los médicos que se enfrentan a este problema. Revisaremos la ventajas y desventajas de la Elastografia hepática de transición Fibroscan en la práctica clínica.
¿Cómo funciona la Elastografia Hepática Fibroscan?
VCTE funciona mediante la medición de la velocidad de onda de corte. En esta técnica, una sonda de mano se coloca en el espacio intercostal superponiendo el lóbulo hepático derecho. La velocidad de las ondas de corte que regresan, medida a una profundidad de 25 a 65 mm, se convierte en una medición de la rigidez del hígado (LSM) mediante el uso de la ley de Hook. La resistencia a la deformación (es decir, rigidez) en un material dado (en este caso un hígado) bajo estrés (una onda de corte) se expresa mediante el módulo de Young en kilopascales (kPa). elastografia hepática fibroscan utiliza la fórmula E = 3 p V 2, que se basa en la ley de Hook, donde E es el módulo de Young, p es la densidad de masa (que se supone 1,000 kg / m 3), y V es la velocidad de la onda de corte 2 ( Figura 1 ). El LSM obtenido a partir de un examen VCTE dado es el valor de la mediana de al menos 10 mediciones de éxito. El éxito se basa en 2 criterios, la calidad de la onda de corte emitida por la sonda y la calidad de la imagen, la velocidad de deformación para estimar la rigidez. LSM se traduce en información clínicamente significativa en relación con los puntos de corte basados en la evidencia pertinente a la condición subyacente del paciente. Sin embargo, estos puntos de corte son arbitrarios en diferentes poblaciones, y el VCTE no determina el estadio de fibrosis sino que estratifica el riesgo y se correlaciona muy bien con la fibrosis.
¿Qué factores o estados patológicos pueden alterar los resultados de la Elastografia hepática Fibroscan ?
Hay algunos temas a tener en cuenta con respecto al rendimiento al utilizar elastografia hepática fibroscan en las múltiples etiologías de la enfermedad hepática. Debido al mecanismo de adquisición de datos, cualquier proceso que interfiere con la profundidad del hígado examinado en relación con la sonda puede afectar el éxito de medición. Por ejemplo, la ascitis se opone a la aplicabilidad de elastografia hepática fibroscan ó VCTE pero es menos crítica para los clínicos que evalúan los pacientes para la enfermedad hepática avanzada. Importantes factores de confusión LSM son la obesidad, la inflamación Hepatitis agudas ), la colestasis, la congestión ( Insuficiencia cardiaca congestiva ) y la ingesta de alimentos o de alcohol recientemente – En estos estados puede el resultado ser un falso positivo.
La reproducibilidad de elastografia hepática fibroscan ha sido examinado por varios grupos por primera vez en 2007 por Fraquelli et al. 3 Este grupo estudió 800 exámenes VCTE, 2.4% de los cuales dieron resultados indeterminados. Los factores asociados significativamente con el resultado entre examinadores incluyen el aumento de índice de masa corporal (IMC) (25 kg / m2 o mayor), esteatosis, grados de fibrosis leves. Del mismo modo, en un estudio de sujetos sanos, la tasa de fracaso VCTE (0 adquisiciones válidos) aumentó con el IMC, alcanzando una tasa de fracaso del 88% para el índice de masa corporal mayor de 40 kg / m 2. 4. Castera et al 5 confirmó estas tendencias y demostró cómo en un estudio posterior examinando 13369 VCTE, las tasas de fracaso y poco fiables de los exámenes (menos de 10 adquisiciones válidos o tasa de éxito <60% o rango intercuartil menos del 30% del valor de la mediana) se produjeron en el 3,1% y el 15,8% de los exámenes, respectivamente. El fracaso fue el más asociado con el índice de masa corporal mayor de 30 kg / m 2 (odds ratio [OR] = 7,5) y la experiencia del operador de menos de 500 exámenes (OR = 2,5). Lo mismo se aplica para los exámenes no fiables: índice de masa corporal mayor de 30 kg / m 2 (OR, 3,3) y la inexperiencia del operador (OR, 3,1). 5
Más allá de la obesidad, esencialmente cualquier proceso que altera las propiedades viscoelásticas hepáticas puede afectar a LSM. La inflamación hepática aguda o crónica, puede conducir a la LSM falsamente elevados. Considerando que la esteatosis por sí sola no afecta VCTE, La esteatohepatitis no lo hace. La colestasis extrahepática, la congestión pasiva cardiogénico o hipertensión venosa central, el depósito de amiloide, y la ingestión de la comida (al menos en pacientes cirróticos) se ha demostrado que influyen en la rigidez hepática medida por VCTE.
Por último, la experiencia del operador puede jugar un papel. En general, los operadores tienen que haber hecho más de 100 exámenes, quizás más que 500, antes de la experiencia del operador ya no es una variable de confusión.
En resumen, hay varios factores que deben ser abordados para garantizar la calidad de la información obtenida a partir de la Elastografia hepática Fibroscan. Actualmente recomendamos al menos 10 mediciones de la rigidez del hígado con un rango intercuartil de <0,3 (IQR /med menor del 30% )y una tasa de éxito superior al 60%. Algunas autoridades recomiendan que al menos el 70% de las mediciones sea válido, pero esto realmente nunca ha sido estudiado y comparado con biopsia hepática. Los pacientes deben tener un ayuno de alimentos durante al menos 3 horas. Debe realizarse una corrección si los niveles de alanina aminotransferasa (ALT) son superiores a 100 UI / L. Por último, se recomienda una historia y examen físico para evaluar la evidencia de las variables de confusión conocidos.
¿Cuál es la utilidad de la Elastografía hepática Fibroscan ?
La verdadera utilidad es determinación no invasiva de la fibrosis y de la cirrosis
El examen diagnóstico patrón oro de larga data de la fibrosis hepática es la biopsia hepática. Es un examen imperfecto con muchas desventajas. Es un procedimiento invasivo que requiere recursos significativos, incluyendo operadores altamente capacitados, cuidados de enfermería para la observación y análisis de la muestra extraída para patología por un patólogo experto. Se asocia con un riesgo potencialmente significativo que va desde dolor a la hemorragia. 19 Por último, las muestras de biopsia de hígado, representan más o menos 1 / 50.000 del hígado, que es naturalmente heterogéneo. 20 El error de muestreo se complica aún más por el acuerdo entre observadores sin experiencia menudo asociada con la interpretación histológica, con discrepancias en cuanto a la estadificación lo cual ocurre hasta en el 58% de las biopsias (dependiendo del grado de fibrosis). 21 22 En la era de las terapias antivirales cada vez más eficaces para nuestros pacientes con la hepatitis, la magnitud de todos estos problemas de riesgo, el coste y la falta de fiabilidad, únicamente incrementa la necesidad de un método diagnóstico conveniente no invasivo .
Las ventajas de la Elastografia hepática Fibroscan sobre la biopsia son varios. Es más seguro y menos costoso y evalúa un volumen mucho mayor de parénquima hepático. En general, los datos muestran que VCTE, no a diferencia de los marcadores serológicos de fibrosis, mejor discierne los extremos de la fibrosis, F0 / F1 frente a F4. Es importante destacar que, independientemente de la etiología, el diagnóstico de la cirrosis VCTE puede con un área bajo la curva de eficacia diagnóstica (curva ROC) de 0,94 (95% intervalo de confianza [IC]: 0,93 a 0,95).
¿Qué utilidad tiene la Elastografia hepática Fibroscan en pacientes con hepatitis C (VHC) ?
la infección crónica por el VHC es a la vez común y un determinante importante de la salud pública en los Estados Unidos. La morbilidad de la infección por VHC es casi completamente relacionada con el desarrollo de la cirrosis. Debido a los Centros para la recomendación de Control de Enfermedades han evaluado a los pacientes nacidos entre 1945 y 1965 para el VHC y la creciente ola de terapias eficaces contra el VHC, debemos anticipar una gran afluencia de pacientes en el orden de 1 millón de personas que buscan atención para el VHC. 1 La elastografia hepática de transición Fibroscan es una excelente opción para estos pacientes, lo que podría resolver el costo y riesgo de la evaluación de la biopsia al tiempo que reduce la vacilación relacionada con el paciente hacia las pruebas de diagnóstico. En consecuencia, es fundamental que los médicos sean capaces de interpretar los resultados de la elastografia hepática fibroscan y conocer sus limitaciones.
Tradicionalmente, la fibrosis en el VHC ha sido puesta en escena mediante el uso de una variedad de sistemas de puntuación; la 2 más comúnmente utilizados son los puntajes de METAVIR y Ishak. 27 28 Estas puntuaciones fueron diseñados para el estadio de fibrosis a través fibrosis portal, fibrosis en puente, y la cirrosis. Su valor fue más significativo para los ensayos clínicos, lo que ayuda a priorizar los pacientes con fibrosis portal o más avanzado que necesita tratamiento y especialmente en la era del interferón cuando los efectos secundarios del tratamiento limitan la aceptabilidad del paciente, las tasas de respuesta fueron más bajos, y muchos pacientes con enfermedad leve desea aplazar el tratamiento . Ahora, la eficacia de los nuevos tratamientos se aproxima a> 90% respuesta virológica sostenida, y el aumento de la tolerabilidad de los regímenes sin interferón ha hecho que la estadificación exacta de la enfermedad sea menos importante. Por lo tanto para el clínico hoy en día, la estadificación exacta de la enfermedad es menos relevante. Los médicos deben utilizar las nuevas tecnologías para identificar a los pacientes con insuficiencia renal leve o sin fibrosis y, por tanto, las posibilidades de eventos relacionados con el hígado de las personas con enfermedad más avanzada. En este nuevo paradigma, el escenario no debe determinar la elegibilidad tratamiento, pero puede ser utilizado en los países con pocos recursos como el nuestro Colombia para determinar las prioridades para la terapia. El conocimiento más importante derivado de la puesta en escena de la fibrosis en el VHC es la identificación de aquellos pacientes con fibrosis en puente y especialmente cirrosis que deben ser examinados para determinar la presencia de varices esofágicas y del carcinoma hepatocelular. En consecuencia, podríamos considerar la etapa más crítica de la fibrosis en escena como la exclusión de cirrosis con el mayor valor predictivo negativo (VPN).
Por lo tanto, utilizamos VCTE como la primera prueba crítica de punto de cuidado para excluir la presencia de cirrosis. Descrita por primera vez por Ziol et al 29 en su estudio prospectivo de elastografia hepática fibroscan comparado con biopsia en 327 pacientes con el VHC, los puntos de corte óptimos para LSM F2 y F4 o mayor (cirrosis) fueron 8,7 y 14,5 kPa, respectivamente. Sin embargo, estudios posteriores han determinado otros puntos de corte. Ese mismo año, Castera et al 24 informó sobre 183 pacientes con VHC consecutivos con valores de corte de 7,1 kPa para ≥F2, 9,5 kPa para ≥F3, y 12,5 kPa para F4. Dos años más tarde, Fraquelli et al 3 identifica los siguientes puntos de corte en una población italiana: 7,9 kPa para ≥F2, 10.3 kPa para ≥F3, y el 11,9 kPa para F4. Arena et al 30 encontró que los pacientes con menos de 12 kPa indican claramente la ausencia de la cirrosis, mientras que un punto de corte de más de 18 kPa indica claramente la cirrosis. Cardoso et al 31 encontraron que el punto de corte de 7,1 kPa tiene un valor de 88% predictivo positivo (VPP) de fibrosis significativa, mientras que el 12,5 kPa tiene un valor presente neto del 98% para la cirrosis. En los Institutos Nacionales de la Salud en su experiencia con VCTE, 7 pacientes con biopsias de falsos negativos y la cirrosis clínica fueron identificados correctamente por un corte de LSM de 13,1 kPa. 32 En nuestras manos, un corte de la rigidez conservadora de 7,3 kPa distingue pacientes estadounidenses sin fibrosis significativa de los que puede con excelente VPN. 7 Recientemente hemos informado de los resultados del estudio de cohorte EE.UU. que incluía nuestra experiencia con más de 900 pacientes estadounidenses con hepatitis viral crónica con un IMC medio de 27,3 kg / m 2. En esta población, los puntos de corte para la fibrosis F3 (puente) fueron 8,5 y 8,6 kPa para los pacientes por encima y por debajo de la mediana del IMC. Los puntos de corte para F4 (cirrosis) fueron 17,1 y 10,4 kPa para los pacientes por encima y por debajo de la mediana del IMC, con la respectiva curva ROC de 0,91 y 0,90. 33
Es importante contextualizar puntos de corte para la fibrosis avanzada por contabilización de las propiedades viscoelásticas de la inflamación crónica. El nivel de ALT se conoce en el momento de elastografia hepática fibroscan . Se ha sabido por mucho tiempo que la inflamación, aguda y crónica, confunde LSM en pacientes con VHB y poblaciones mixtas de hepatitis viral. 8 34 35 En 2012, se informó en este diario que en un grupo de pacientes con fibrosis F0-F2 confirmado por biopsia, LSM sugerentes de la cirrosis por 3 puntos de corte diferentes 3 24 29 se obtuvieron en pacientes con inflamación histológica de alta calidad, así como en aquellos con ALT alta. Utilizando el punto de corte más conservador, 29 niveles de ALT por encima de 80 y 120 UI / L sugirió un hígado «cirrótico» con OR de 3,84 y 4,10, respectivamente. 7 Estos resultados están apoyados además por la disminución de la rigidez del hígado que los pacientes experimentan durante la terapia antiviral para VHC. 36 37.
¿Qué utilidad tiene la Elastografia hepática Fibroscan en pacientes con hepatitis B (VHB) ?
La experiencia con VCTE en VHB se ha quedado atrás hasta hace poco de VHC . Desde varios grupos franceses con experiencia VCE conocida llegó algunos de los primeros datos más fuertes. Marcelino et al 38 llevaron a un grupo multicéntrico que evaluó prospectivamente 202 pacientes con biopsia emparejado y LSM. El porcentaje fue de 0,81 y 0,93 para ≥F2 y F4. Sus valores de corte óptimo LSM fueron 7,2 y 11,0 kPa para ≥F2 y F4, respectivamente. Mediante el uso de puntos de corte de 11,0 y 18,2 kPa, los respectivos VPP / VPN para la cirrosis fueron del 38% / 99% frente a 67% / 96%. El rendimiento de estos puntos de corte se ha confirmado en manos de otros. 31 Un reciente meta-análisis de estudios publicados que comprenden a 2772 pacientes, se evaluó el rendimiento de la elastografia hepática Fibroscan en VHB crónica. Catorce de los 18 estudios incluidos en este análisis eran estrictamente VHB exclusiva. Los puntos de corte para la F2 (o mayor), F3-F4 y F4 fueron 7,9 kPa, 8,8 kPa y 11,7 kPa, respectivamente. Un LSM de 11,7 kPa tuvo una sensibilidad del 84,6% y una especificidad del 81,5% para la detección de la cirrosis. 39
Tanto en HBV como en HCV, existe la posibilidad de un aumento de falsos positivos en la rigidez hepática medida como resultado de la actividad necroinflamatoria. 40 Una de las primeras señales de que la inflamación crónica, reflejada por el nivel de ALT, afectado fiabilidad de la Elastografía hepática Fibroscan en VHB provino del estudio de Oliveri et al 8 de 297 pacientes italianos consecutivos con VHB crónica. Entre los pacientes con fibrosis etapa idéntica, aquellos con niveles elevados de ALT tuvieron mayor LSM. LSM también aumentó 1,3 veces a 3 veces durante los brotes de VHB detectado durante la evaluación. Este hallazgo es más fácilmente reproducibles, totalmente inadecuada en un grupo de 12 pacientes cirróticos con VHB aguda. 6 9 41 Nueve de sus pacientes (75%) tenían LSM mayor que 11,9 kPa en la presentación, lo que sugiere la cirrosis. En la semana 24 después de la resolución de la hepatitis aguda, ninguno tenía LSM superior a 11,9 kPa. 41 Para determinar la contribución relativa a la rigidez del hígado de cada nivel de actividad viral, Fung et al 42 evaluaron prospectivamente 157 pacientes en Hong Kong. VCTE se realizó en sujetos sanos, así como en aquellos con HBV oculta (la carga viral positiva, antígeno de superficie negativa), HBV activo (antígeno de superficie positivo y la carga viral), y HBV-cirrosis. Los LSM respectivas de estos grupos fueron 4,6 kPa (2,0 a 7,1), 4,2 kPa (3.4 a 6.9), 8.7 kPa (3,6 a 44,3) y 33,8 kPa (11,9-75). Claramente, ALT puede confundir PPV de VCTE y debe considerarse al interpretar sus resultados.
Debido a las directrices explícitamente se basan las recomendaciones de tratamiento del VHB en la inflamación (ALT), la carga viral, y con frecuencia la histología, el efecto de confusión de la ALT tiene una dimensión añadida de importancia. De acuerdo con ello, Chan et al 43 sugieren un algoritmo basado en ALT para el uso de VCTE en HBV. Sobre la base de su experiencia con 161 pacientes chinos sometidos VCTE emparejado y biopsia, este grupo sugiere que cuando los pacientes tienen una puntuación normal ALT por encima o por debajo de los puntos de corte VCTE para la fibrosis significativa (en su estudio 5 kPa o menos frente a 9,0 kPa o mayor), uno puede tomar decisiones de tratamiento sin una biopsia de hígado, reservando la biopsia de pacientes con resultados indeterminados (por ejemplo, 6-9 kPa). Sin embargo, para los pacientes con ALT elevada (mayor que el límite superior de lo normal), se utilizó la biopsia hepática en una zona indeterminada expandida de 7 a 12 kPa. 43 En la práctica clínica, se podría sustituir la biopsia para la evaluación serológica de la fibrosis (Figura 2).
¿Qué utilidad tiene la Elastografia hepática Fibroscan en pacientes con enfermedad hígado graso no alcoghólico (EHNA) y en esteatohepatitis no alcohólica ( NASH ) ?
El Hígado graso no alcohólico es prevalente en el 46% de los estadounidenses y la esteatohepatitis no alcohólica (NASH) en más de un 12%, y las tasas están aumentando de manera significativa a nivel mundial. 44 45 Debido al tamaño de la población con hígado graso no alcohólico, existen preocupaciones legítimas de salud pública en relación con el costo y riesgo de la evaluación de la biopsia para la enfermedad avanzada. La biopsia se utiliza para el estadio de fibrosis y para diferenciar la esteatosis simple a partir de NASH, y nuevos sistemas de puntuación propuesto para diagnosticar NASH se basan en la esteatosis, la inflamación y apoptosis. 46 Dado que el APV no puede diferenciar de forma fiable las características histológicas de la EHNA, debe tenerse en cuenta que el APV sólo se puede utilizar para determinar el grado de fibrosis o presencia de cirrosis y no a diagnosticar o descartar la EHNA. 47 Los principales problemas que afectan a la Elastografia hepática Fibroscan en hígado graso no alcohólico son un aumento en los exámenes fallidos o sesgados debido a índice de masa corporal elevados o potencialmente debido a la confusión por la esteatosis. 44 La razón más común para el fracaso de VCTE es un índice de masa corporal mayor de 30 kg / m 2, en donde la tasa de fracaso es informado de 22% -25%. 48 49
El efecto de la esteatosis en la rigidez del hígado es controvertida, pero varios estudios han explorado esta relación. Por ejemplo, Gaia et al 50 encontró que los pacientes con NAFLD con F3 y esteatosis severa tenían valores de LSM inferiores, similares a los de los pacientes con F1 y esteatosis leve. Mediante el uso de un corte de 8 kPa, la elastografia hepática Fibroscan subestimó el estadio de fibrosis en el 75% de los pacientes con esteatosis F3 y severa. Sin embargo, mediante el uso de un corte similar de 8,75 kPa para ≥F3 la fibrosis, Petta et al 51 encontraron una tasa de falsos negativos del 24%. En el estudio más grande, Wong et al 48 estudiaron prospectivamente 246 pacientes consecutivos a partir de centros en China y Francia, y mediante el uso de un corte de 10,3 kPa, se encontraron con un 99% y un 46% VAN PPV para el diagnóstico de la cirrosis.
La llamada sonda XL fue diseñado para superar la adiposidad de la pared torácica y mejorar las características de prueba de la elastografia hepática Fibroscan en una población obesa. Hay evidencia de que su funcionamiento es reproducible. En comparación con la sonda M, la sonda XL tiene un diámetro mayor en la punta, menor frecuencia central, y una mayor amplitud de vibración. Críticamente, se evalúa la rigidez del hígado a mayor profundidad (3.5-7.5 cm). Los pacientes obesos pueden experimentar tasas similares de de éxito de LSM cuando se utiliza esta sonda modificada. 52 53 54 55 Por ejemplo, Myers et al 54 han demostrado en una población de 276 pacientes con enfermedad hepática crónica y el IMC> 28 kg / m 2, que la tasa de fracaso fue significativamente menor con la sonda XL que con la sonda M (1,1% frente al 16%; p <0,00005). Sin embargo, siguen siendo cuestionables 2. En primer lugar, incluso con la sonda XL, aunque en menor grado que la sonda M, la fiabilidad de Elastografia hepática de transicion disminuye para los pacientes con un IMC mayor de 30 kg / m 2. 53 Asimismo, los resultados poco fiables aún se observan con la sonda XL en 25% de los casos en comparación con el 50% de los casos con la sonda M (p <0,00005). 54 En efecto, la sonda XL y la histología son discordantes en hasta el 9% de los pacientes con un IMC mayor de 35 kg / m 2. 49 En segundo lugar, la sonda XL puede generar LSM más baja que la sonda anterior M en el mismo paciente, lo que sugiere que los puntos de corte de fibrosis específicos de la enfermedad pueden necesitar ser más baja en los exámenes de sonda XL. Múltiples investigadores han encontrado que LSM por la sonda XL es menor que por la sonda M por tanto como 1,7 + 2,3 kPa. 49 54 Por lo tanto, aunque estas nuevas sondas mejorar la fiabilidad de VCTE en pacientes obesos, se necesita más investigación para determinar el IMC puntos de corte para la confiabilidad y precisión.
¿Qué utilidad tiene la Elastografia hepática Fibroscan en enfermedad hepática alcohólica?
Enfermedad hepática alcohólica y Elastografia hepática fibroscan
Especialmente en sus primeras etapas, la enfermedad hepática alcohólica se caracteriza por fibrosis sinusoidal, la esteatosis y la inflamación significativa; por lo tanto, por LSM VCTE es susceptible a los factores de confusión. La abstinencia puede afectar dramáticamente los resultados VCTE. Reproducible, la abstinencia se asocia con una disminución más o menos 4,9 kPa en LSM, la reducción significativa LSM se puede ver incluso después de 7 días de abstinencia. LSM disminuyó desde 7,2 hasta 6,1 kPa en 7 días de sobriedad en un estudio, lo que resulta en una reducción en la etapa de fibrosis estimado en 32 pacientes (23,3%). Nahon et al examinó el papel de VCTE en una población francesa de 147 pacientes con enfermedad hepática alcohólica que se someten emparejados LSM y la biopsia, el 53,7% de los cuales tenía cirrosis y el 28,7% de los cuales tenían moderada a marcada hepatitis alcohólica en la biopsia. Mediante el uso de puntos de corte óptimos de 12,96 y 22,7 kPa, las AUROCs eran 0,94 y 0,87 para el diagnóstico de fibrosis avanzada y cirrosis, respectivamente. Con exclusión de los pacientes que estaban tomando activamente, Mueller et al encontró que un corte de 12,5 kPa tenía una curva ROC de 0,91 para la fibrosis F4. Por lo tanto, cuando se utiliza la elastografia hepática Fibroscan para evaluar pacientes con enfermedad hepática alcohólica, el médico debe tener en cuenta tanto los hábitos de consumo actuales y la presencia de la esteatohepatitis alcohólica activa. Se recomienda 7 días de abstinencia al alcohol y una ALT por debajo de 100 ui/dl. Además al momento de interpretar los resultados luego de 7 dias de abstinencia el rango o nivel asociado a cirrosis en éstos pacientes es muy superior estando por encima de 17.5 kPa.
Enfermedad biliar y elastografia hepática fibroscan
La experiencia con elastografia hepática fibroscan en el entorno de la enfermedad hepática biliar primaria es limitada. La colestasis extrahepática se sabe que aumenta la rigidez del hígado para todos los pacientes. 11 Corpechot et al 61 fueron el primer grupo para examinar el papel de elastografia hepática fibroscan en la cirrosis biliar primaria (CBP) y colangitis esclerosante primaria. En su estudio prospectivo multicéntrico, 73 pacientes con cirrosis biliar primaria y 28 con colangitis esclerosante primaria fueron sometidos emparejados elastografia hepática fibroscan y biopsia hepática. Las predicciones para AUROCs LSM del estadio de fibrosis fueron 0,92 y 0,96 para ≥F2 y F4, respectivamente. los valores de corte de rigidez óptimas para la fibrosis avanzada (F3-F4) y la cirrosis fueron del 9,8 y el 17,3 kPa, respectivamente. Un LSM de 9,8 kPa se asoció con OR de 72,7 (IC del 95%, 11,0 a 1488,2) para la presencia de fibrosis avanzada. Friedrich-Rust et al 62 en comparación con elastografia hepática fibroscan espectroscopia de resonancia magnética y los marcadores séricos en un grupo de 45 alemanes con PBC con biopsias hepáticas pareadas. VCTE proporcionado correlación superior con la histología: AUROCs de 0,74 y 0,95 para ≥F2 y fibrosis F4, respectivamente. Recientemente, Corpechot et al examinó el papel de elastografia hepática fibroscan en la evaluación longitudinal de los pacientes con PBC tratados con ácido ursodesoxicólico. Encontraron una tasa de progresión global de 0,48 ± 0,21 kPa / año, pero no detectaron ninguna progresión en las etapas de METAVIR.
Elastografia hepática fibroscan para la predicción de los resultados relacionados con el hígado
Es intuitivo que el aumento de la rigidez del hígado refleja el aumento de la hipertensión portal. elastografia hepática fibroscan puede predecir la hipertensión portal significativa (gradiente de presión venosa hepática ≥10 mm Hg), la presencia de varices, y el riesgo de hemorragia varicosa, pero no se recomienda como un sustituto de la endoscopia. 64 Un reciente meta-análisis encontró un VPP y VPN combinada del 88% de la capacidad de elastografia hepática fibroscan para predecir la presencia de hipertensión portal significativa. 65 En el mayor estudio para examinar esta cuestión, Bureau et al 66 estudiaron prospectivamente 150 pacientes consecutivos franceses sometidos a biopsia hepática transyugular y la medición de la presión portal, el 59% de los cuales eran cirróticos. El control de la ALT, aspartato aminotransferasa, la albúmina, la razón normalizada internacional, y el recuento de plaquetas, LSM ≥21 kPa tenía OR de 120,4 para el gradiente de presión venosa hepática ≥10 mm Hg. Un punto de corte de 11,7 kPa tenido VPP y VPN del 77,4% y 93,1%, respectivamente, mientras que el 21,0 kPa tenía VPP y VPN del 92,5% y 90,7%, respectivamente. En un estudio retrospectivo de 124 estadounidenses con cirrosis que fueron sometidos a endoscopia de los cuales 63 tenían varices esofágicas, nuestro grupo encontró que un corte de la rigidez del hígado, de 20 kPa por VCTE produjo VPP y VPN de varices de 80% y 75%, respectivamente. La elastosonografia hepática ha demostrado ser tan eficaz como el gradiente hepático de presión venosa en la predicción de descompensación clínica en pacientes cirróticos. 68 En un estudio, el gradiente de presión venosa hepática ≥10 mm Hg y LSM ≥21.1 kPa tenían 100% VAN para complicaciones de la hipertensión portal. 68 En un grupo de 1000 rumanos con cirrosis, un punto de corte de 50,7 kPa tenía 82.71% 53.66% VPP y VPN para la predicción de sangrado esofágico. 69
Dado un paso más, puede haber un papel para la medición por elastografia FibroScan serie en pacientes con cirrosis. Corpechot et al 63 descubrieron que en los pacientes cirróticos con PBC que fueron seguidos con medición anual, el aumento de la rigidez hepática se asociao fuertemente con los resultados clínicos como la descompensación, el trasplante de hígado o la muerte. Del mismo modo, en una cohorte de 128 pacientes coreanos con cirrosis por VHB activo, un punto de corte de 19 kPa produjo un riesgo relativo de 7.176 para el desarrollo de descompensación clínica, incluyendo el carcinoma hepatocelular. 70
Este examen no invasivo es de hecho una herramienta robusta que predice de manera reproducible una descompensación hepática. En un grupo de 667 pacientes con hepatitis viral crónica que fueron seguidos durante 861 días, 57 pacientes murieron o ascitis, encefalopatía, hemorragia varicosa, carcinoma hepatocelular, o la cotización para el trasplante desarrollados. En general, elastografia posee curva ROC de 0,87, y un punto de corte de 10,5 kPa tenido VPN del 99,2% para la predicción de estos resultados importantes. 71 Singh et al 72 recientemente realizó un meta-análisis de todos los estudios que examinan la capacidad de predicción del FibroScan por descompensación de la enfermedad hepática crónica. Por cada kilopascales sobre el LSM medio determinado, un determinado paciente tiene un mayor riesgo relativo de un evento clínico importante: 1.07 de descompensación hepática, 1,11 para el carcinoma hepatocelular, y 1,22 para la muerte.
Una nueva aplicación para VCTE es la medición del bazo rigidez, que también tiene como objetivo predecir eventos con hipertensión portal. rigidez Spleen es una técnica en investigación cuando se consideran reflectante de la congestión esplénica las mediciones de rigidez bazo. Más estudios para delinear sus limitaciones, así como la gama de rigidez bazo normales son necesarios antes los médicos deben adoptar esta técnica. En primer lugar reportado en 2011, Stefanescu et al 73 encontraron en su estudio retrospectivo en el que un punto de corte óptimo de 52,5 kPa rindió curva ROC de 0,74 para la predicción de la presencia de varices. El estudio prospectivo de Collecchia et al 74 se obtuvo resultados similares. En un estudio prospectivo de 174 pacientes de la India, entre los pacientes con varices, rigidez bazo fue significativamente mayor en los pacientes que tenían varices grandes (56 frente a 49 kPa) y un historial de sangrado por várices (58 vs 50,2). 75
La atenuación controlada de parámetros para estadificación del Hígado Graso utilizan el CAP
Una nueva técnica desarrollada por el uso de VCTE a la etapa esteatosis se denomina parámetro de atenuación controlada (CAP). Es un algoritmo patentado que se basa en el coeficiente de atenuación ultrasónica de onda de corte de VCTE, una estimación de la atenuación ultrasónica total de (ir y vuelta ruta) a 3,5 MHz. CAP utiliza los mismos datos de radiofrecuencia como LSM y sólo se aprecia si la adquisición es válida. Se expresa en decibelios por metro. En el informe original, junto con la histología CAP tenía curva ROC de 0,91, 0,95, y 0,89 para las etapas de esteatosis 1, 2, y 3, respectivamente. Cuando se evaluó después en 615 pacientes con hepatitis C crónica por el mismo grupo, CAP tenían curva ROC de 0,80, 0,86 y 0,88 para las etapas 1, 2 y 3, respectivamente. Debido a que la esteatosis es un marcador reversible que refleja el potencial de daño hepático más, CAP es una herramienta de investigación prometedora para que los médicos aconsejan a los pacientes sobre los riesgos futuros y estrategias terapéuticas.
La incorporación de la elastografia hepática fibroscan en la práctica
El uso juicioso de elastografia hepática fibroscan incluye la selección de candidatos apropiados o al menos reconocer los factores importantes para realizar una buena interpretación de los resultados. Como mínimo, esto implica saber la enfermedad de base del paciente, índice de masa corporal (obesidad), ALT (inflamación), fosfatasa alcalina (colestasis), y si está ayunando. A partir de entonces, se recomienda que elastografia hepática fibroscan se realiza conjuntamente con una evaluación de marcadores serológicos de fibrosis, tales como el Fibrotest, Hepascore, FIB4, o APRI. 78 79 pruebas concordantes se consideran mutuamente confirmatorio, mientras que las pruebas discordantes se pueden repetir en una fecha posterior y biopsias dejaron solamente para pacientes en los resultados discordantes permanecen sin resolver (Figura 3).
El FibroScan se puede utilizar después de una buena historia clínica para predecir en grado de enfermedad hepática crónica como método de cribado tanto en poblaciones de riesgo como en general.
Debido a la pandemia COVID 19 los índices de enfermedad hepática crónica y alteración de enzimas hepáticas dado al aumento del sobrepeso y la obesidad como pruebas de cribado y seguimiento deben ser tenido en cuenta .
Bibliografias:
- Recommendations for the identification of chronic hepatitis C virus infection among persons born during 1945–1965. MMWR 2012; 61: pp. 1-18
- Sandrin L., Fourquet B., Hasquenoph J.M., et al: Transient elastography: a new noninvasive method for assessment of hepatic fibrosis. Ultrasound Med Biol 2003; 29: pp. 1705-1713
- Fraquelli M., Rigamonti C., Casazza G., et al: Reproducibility of transient elastography in the evaluation of liver fibrosis in patients with chronic liver disease. Gut 2007; 56: pp. 968-973
- Roulot D., Czernichow S., Le Clésiau H., et al: Liver stiffness values in apparently healthy subjects: influence of gender and metabolic syndrome. J Hepatol 2008; 48: pp. 606-613
- Castéra L., Foucher J., Bernard P.H., et al: Pitfalls of liver stiffness measurement: a 5-year prospective study of 13,369 examinations. Hepatology 2010; 51: pp. 828-835
- Sagir A., Erhardt A., Schmitt M., et al: Transient elastography is unreliable for detection of cirrhosis in patients with acute liver damage. Hepatology 2008; 47: pp. 592-595
- Tapper E.B., Cohen E.B., Patel K., et al: Levels of alanine aminotransferase confound use of transient elastography to diagnose fibrosis in patients with chronic hepatitis C virus infection. Clin Gastroenterol Hepatol 2012; 10: pp. 932-937
- Oliveri F., Coco B., Ciccorossi P., et al: Liver stiffness in the hepatitis B virus carrier: a non-invasive marker of liver disease influenced by the pattern of transaminases. World J Gastroenterol 2008; 14: pp. 6154-6162
| - Arena U., Vizzutti F., Corti G., et al: Acute viral hepatitis increases liver stiffness values measured by transient elastography. Hepatology 2008; 47: pp. 380-384
- Kim K.M., Choi W.B., Park S.H., et al: Diagnosis of hepatic steatosis and fibrosis by transient elastography in asymptomatic healthy individuals: a prospective study of living related potential liver donors. J Gastroenterol 2007; 42: pp. 382-388
- Millonig G., Reimann F.M., Friedrich S., et al: Extrahepatic cholestasis increases liver stiffness (FibroScan) irrespective of fibrosis. Hepatology 2008; 48: pp. 1718-1723
- Lebray P., Varnous S., Charlotte F., et al: Liver stiffness is an unreliable marker of liver fibrosis in patients with cardiac insufficiency. Hepatology 2008; 48: pp. 2089
- Millonig G., Friedrich S., Adolf S., et al: Liver stiffness is directly influenced by central venous pressure. J Hepatol 2010; 52: pp. 206-210
- Bordessoule D., Vidal E., Sautereau D., et al: Non-invasive detection of hepatic amyloidosis: FibroScan, a new tool. Amyloid 2011; 18: pp. 19-24
- Berzigotti A., De Gottardi A., Vukotic R., et al: Effect of meal ingestion on liver stiffness in patients with cirrhosis and portal hypertension. PLoS One 2013; 8: pp. e58742
- Mederacke I., Wursthorn K., Kirschner J., et al: Food intake increases liver stiffness in patients with chronic or resolved hepatitis C virus infection. Liver Int 2009; 29: pp. 1500-1506
- Arena U., Lupsor Platon M., Stasi C., et al: Liver stiffness is influenced by a standardized meal in patients with chronic HCV hepatitis at different stages of fibrotic evolution. Hepatology 2013; 58: pp. 65-72
- Kettaneh A., Marcellin P., Douvin C., et al: Features associated with success rate and performance of FibroScan measurements for the diagnosis of cirrhosis in HCV patients: a prospective study of 935 patients. J Hepatol 2007; 46: pp. 628-634
- Seeff L.B., Everson G.T., Morgan T.R., et al: Complication rate of percutaneous liver biopsies among persons with advanced chronic liver disease in the HALT-C trial. Clin Gastroenterol Hepatol 2010; 8: pp. 877-883
- Bravo A.A., Sheth S.G., and Chopra S.: Liver biopsy. N Engl J Med 2001; 344: pp. 495-500
- Robert M., Sofair A.N., Thomas A., et al: A comparison of hepatopathologists’ and community pathologists’ review of liver biopsy specimens from patients with hepatitis C. Clin Gastroenterol Hepatol 2009; 7:
- Bedossa P., Dargère D., and Paradis V.: Sampling variability of liver fibrosis in chronic hepatitis C. Hepatology 2003; 38: pp. 1449-1457
- Friedrich-Rust M., Ong M.F., Martens S., et al: Performance of transient elastography for the staging of liver fibrosis: a meta-analysis. Gastroenterology 2008; 134: pp. 960-974
- Castéra L., Vergniol J., Foucher J., et al: Prospective comparison of transient elastography, Fibrotest, APRI, and liver biopsy for the assessment of fibrosis in chronic hepatitis C. Gastroenterology 2005; 128: pp. 343-350
- Zarski J.P., Sturm N., Guechot J., et al: Comparison of nine blood tests and transient elastography for liver fibrosis in chronic hepatitis C: the ANRS HCEP-23 study. J Hepatol 2012; 56: pp. 55-62
- Castera L.: Noninvasive methods to assess liver disease in patients with hepatitis B or C. Gastroenterology 2012; 142: pp. 1293-1302
- Intraobserver and interobserver variations in liver biopsy interpretation in patients with chronic hepatitis C. Hepatology 1994; 20: pp. 15-20
- Ishak K., Baptista A., Bianchi L., et al: Histological grading and staging of chronic hepatitis. J Hepatol 1995; 22: pp. 696-699
- Ziol M., Handra-Luca A., Kettaneh A., et al: Noninvasive assessment of liver fibrosis by measurement of stiffness in patients with chronic hepatitis C. Hepatology 2005; 41: pp. 48-54
- Arena U., Vizzutti F., Abraldes J.G., et al: Reliability of transient elastography for the diagnosis of advanced fibrosis in chronic hepatitis C. Gut 2008; 57: pp. 1288-1293
- Cardoso A.C., Carvalho-Filho R.J., Stern C., et al: Direct comparison of diagnostic performance of transient elastography in patients with chronic hepatitis B and chronic hepatitis C. Liver Int 2012; 32: pp. 612-621
- Gara N., Zhao X., Kleiner D.E., et al: Discordance among transient elastography, aspartate aminotransferase to platelet ratio index, and histologic assessments of liver fibrosis in patients with chronic hepatitis C. Clin Gastroenterol Hepatol 2013; 11: pp. 303-308
- Afdhal N.H., Bacon B.R., Patel K., et al: Diagnosis accuracy of liver stiffness (FibroScan®) in patients with chronic viral hepatitis: results of a large USA cohort. Hepatology 2013; 58: pp. 278A-279A
- Coco B., Oliveri F., Maina A.M., et al: Transient elastography: a new surrogate marker of liver fibrosis influenced by major changes of transaminases. J Viral Hepat 2007; 14: pp. 360-369
- Wong G.L., Wong V.W., Choi P.C., et al: Assessment of fibrosis by transient elastography compared with liver biopsy and morphometry in chronic liver diseases. Clin Gastroenterol Hepatol 2008; 6: pp. 1027-1035
- Verignol J., Foucher J., Castéra L., et al: Changes of non-invasive markers and FibroScan values during HCV treatment. J Viral Hepat 2009; 16: pp. 132-140
- Hézode C., Castéra L., Roudot-Thoraval F., et al: Liver stiffness diminishes with antiviral response in chronic hepatitis C. Aliment Pharmacol Ther 2011; 34: pp. 656-663
- Marcellin P., Ziol M., Bedossa P., et al: Non-invasive assessment of liver fibrosis by stiffness measurement in patients with chronic hepatitis B. Liver Int 2009; 29: pp. 242-247
- Chon Y.E., Choi E.H., Song K.J., et al: Performance of transient elastography for the staging of liver fibrosis in patients with chronic hepatitis B: a meta-analysis. PLoS One 2012; 7: pp. e44930
- Kim S.U., Seo Y.S., Cheong J.Y., et al: Factors that affect the diagnostic accuracy of liver fibrosis measurement by Fibroscan in patients with chronic hepatitis B. Aliment Pharmacol Ther 2010; 32: pp. 498-505
- Viganò M., Massironi S., Lampertico P., et al: Transient elastography assessment of the liver stiffness dynamics during acute hepatitis B. Eur J Gastroenterol Hepatol 2010; 22: pp. 180-184
- Fung J., Lai C.L., Chan S.C., et al: Correlation of liver stiffness and histological features in healthy persons and in patients with occult hepatitis B, chronic active hepatitis B, or hepatitis B cirrhosis. Am J Gastroenterol 2010; 105: pp. 1116-1122
- Chan H.L., Wong G.L., Choi P.C., et al: Alanine aminotransferase-based algorithms of liver stiffness measurement by transient elastography (Fibroscan) for liver fibrosis in chronic hepatitis B. J Viral Hepat 2009; 16: pp. 36-44
- Festi D., Schiumerini R., Marzi L., et al: Review article: the diagnosis of non-alcoholic fatty liver disease—availability and accuracy of non-invasive methods. Aliment Pharmacol Ther 2013; 37: pp. 392-400
- Chalasani N., Younossi Z., Lavine J.E., et al: The diagnosis and management of non-alcoholic fatty liver disease: practice guideline by the American Association for the Study of Liver Diseases, American College of Gastroenterology, and the American Gastroenterological Association. Hepatology 2012; 55: pp. 2005-2023
- Kleiner D.E., and Brunt E.M.: Nonalcoholic fatty liver disease: pathologic patterns and biopsy evaluation in clinical research. Semin Liver Dis 2012; 32: pp. 3-13
- Castera L., Vilgrain V., and Angulo P.: Non invasive evalutation of NAFLD. Nat Rev Gastroenterol Hepatol 2013; 10: pp. 666-675
- Wong V.W., Vergniol J., Wong G.L., et al: Diagnosis of fibrosis and cirrhosis using liver stiffness measurement in nonalcoholic fatty liver disease. Hepatology 2010; 51: pp. 454-462
- Wong V.W., Vergniol J., Wong G.L., et al: Liver stiffness measurement using XL probe in patients with nonalcoholic fatty liver disease. Am J Gastroenterol 2012; 107: pp. 1862-1871
- Gaia S., Carenzi S., Barilli A.L., et al: Reliability of transient elastography for the detection of fibrosis in non-alcoholic fatty liver disease and chronic viral hepatitis. J Hepatol 2011; 54: pp. 64-71
- Petta S., Di Marco V., Cammà C., et al: Reliability of liver stiffness measurement in non-alcoholic fatty liver disease: the effects of body mass index. Aliment Pharmacol Ther 2011; 33: pp. 1350-1360
- De Ledinghen V., Vergniol J., Foucher J., et al: Feasibility of liver transient elastography with FibroScan using a new probe for obese patients. Liver Int 2010; 30: pp. 1043-1048
- De Lédinghen V., Wong V.W., Vergniol J., et al: Diagnosis of liver fibrosis and cirrhosis using liver stiffness measurement: comparison between M and XL probe of FibroScan®. J Hepatol 2012; 56: pp. 833-839
- Myers R.P., Pomier-Layrargues G., Kirsch R., et al: Feasibility and diagnostic performance of the FibroScan XL probe for liver stiffness measurement in overweight and obese patients. Hepatology 2012; 55: pp. 199-208
- Friedrich-Rust M., Hadji-Hosseini H., Kriener S., et al: Transient elastography with a new probe for obese patients for non-invasive staging of non-alcoholic steatohepatitis. Eur Radiol 2010; 20: pp. 2390-2396
- Bardou-Jacquet E., Legros L., Soro D., et al: Effect of alcohol consumption on liver stiffness measured by transient elastography. World J Gastroenterol 2013; 19: pp. 516-522|
- Mueller S., Millonig G., Sarovska L., et al: Increased liver stiffness in alcoholic liver disease: differentiating fibrosis from steatohepatitis. World J Gastroenterol 2010; 16: pp. 966-972
- Gelsi E., Dainese R., Truchi R., et al: Effect of detoxification on liver stiffness assessed by Fibroscan® in alcoholic patients. Alcohol Clin Exp Res 2011; 35: pp. 566-570
- Trabut J.B., Thépot V., Nalpas B., et al: Rapid decline of liver stiffness following alcohol withdrawal in heavy drinkers. Alcohol Clin Exp Res 2012; 36: pp. 1407-1411
- Nahon P., Kettaneh A., Tengher-Barna I., et al: Assessment of liver fibrosis using transient elastography in patients with alcoholic liver disease. J Hepatol 2008; 49: pp. 1062-1068
- Corpechot C., El Naggar A., Poujol-Robert A., et al: Assessment of biliary fibrosis by transient elastography in patients with PBC and PSC. Hepatology 2006; 43: pp. 1118-1124
- Friedrich-Rust M., Müller C., Winckler A., et al: Assessment of liver fibrosis and steatosis in PBC with FibroScan, MRI, MR-spectroscopy, and serum markers. J Clin Gastroenterol 2010; 44: pp. 58-65
- Corpechot C., Carrat F., Poujol-Robert A., et al: Noninvasive elastography-based assessment of liver fibrosis progression and prognosis in primary biliary cirrhosis. Hepatology 2012; 56: pp. 198-208
- Castera L., Pinzani M., and Bosch J.: Non invasive evaluation of portal hypertension using transient elastography. J Hepatol 2012; 56: pp. 696-703
- Shi K.Q., Fan Y.C., Pan Z.Z., et al: Transient elastography: a meta-analysis of diagnostic accuracy in evaluation of portal hypertension in chronic liver disease. Liver Int 2013; 33: pp. 62-71
- Bureau C., Metivier S., Peron J.M., et al: Transient elastography accurately predicts presence of significant portal hypertension in patients with chronic liver disease. Aliment Pharmacol Ther 2008; 27: pp. 1261-1268
- Malik R., Lai M., Sadiq A., et al: Comparison of transient elastography, serum markers and clinical signs for the diagnosis of compensated cirrhosis. J Gastroenterol Hepatol 2010; 25: pp. 1562-1568
- Robic M.A., Procopet B., Métivier S., et al: Liver stiffness accurately predicts portal hypertension related complications in patients with chronic liver disease: a prospective study. J Hepatol 2011; 55: pp. 1017-1024
- Sporea I., Raţiu I., Sirli R., et al: Value of transient elastography for the prediction of variceal bleeding. World J Gastroenterol 2011; 17: pp. 2206-2210
- Kim S.U., Lee J.H., Kim D.Y., et al: Prediction of liver-related events using fibroscan in chronic hepatitis B patients showing advanced liver fibrosis. PLoS One 2012; 7: pp. e36676
- Klibansky D.A., Mehta S.H., Curry M., et al: Transient elastography for predicting clinical outcomes in patients with chronic liver disease. J Viral Hepat 2012; 19: pp. e184-e193
- Singh S., Fujii L.L., Murad M.H., et al: Liver stiffness is associated with risk of decompensation, liver cancer, and death in patients with chronic liver diseases: a systematic review and meta-analysis. Clin Gastroenterol Hepatol 2013; 11: pp. 1573-1584
- Stefanescu H., Grigorescu M., Lupsor M., et al: Spleen stiffness measurement using fibroscan for the noninvasive assessment of esophageal varices in liver cirrhosis patients. J Gastroenterol Hepatol 2011; 26: pp. 164-170
- Colecchia A., Montrone L., Scaioli E., et al: Measurement of spleen stiffness to evaluate portal hypertension and the presence of esophageal varices in patients with HCV-related cirrhosis. Gastroenterology 2012; 143: pp. 646
- Sharma P., Kirnake V., Tyagi P., et al: Spleen stiffness in patients with cirrhosis in predicting esophageal varices. Am J Gastroenterol 2013; 108: pp. 1101-1107
- Sasso M., Tengher-Barna I., Ziol M., et al: Novel controlled attenuation parameter for noninvasive assessment of steatosis using Fibroscan®: validation in chronic hepatitis C. J Viral Hepat 2012; 19: pp. 244-253
- Sasso M., Beaugrand M., de Ledinghen V., et al: Controlled attenuation parameter (CAP): a novel VCTE™ guided ultrasonic attenuation measurement for the evaluation of hepatic steatosis—preliminary study and validation in a cohort of patients with chronic liver disease from various causes. Ultrasound Med Biol 2010; 36: pp. 1825-1835
- Becker L., Salameh W., Sferruzza A., et al: Validation of hepascore, compared with simple indices of fibrosis, in patients with chronic hepatitis C virus infection in United States. Clin Gastroenterol Hepatol 2009; 7: pp. 696-701
- Bonder A., and Afdhal N.H.: Biopsy no more: changing the screening and diagnostic algorithm for hepatitis C. Clin Gastroenterol Hepatol 2013; 11: pp. 309-310
- Castera L., Denis J., Babany G., et al: Evolving practices of non-invasive markers of liver fibrosis in patients with chronic hepatitis C in France: time for new guidelines? J Hepatol 2007; 46: pp. 528-529
- Haute Autorité de Santé. Noninvasive methods for the evaluation of hepatic fibrosis/ cirrhosis: an update. Available at:http://www.has-sante.fr. Accessed August 2008.
- Mutimer D., Aghemo A., Diepolder H., et al: EASL Clinical Practice Guidelines: management of hepatitis C virus infection. J Hepatol 2014; 60: pp. 392-420
- Degos F., Perez P., Roche B., et al: Diagnostic accuracy of FibroScan and comparison to liver fibrosis biomarkers in chronic viral hepatitis: a multicenter prospective study (the FIBROSTIC study). J Hepatol 2010; 53: pp. 1013-1021
- Roulot D., Costes J.L., Buyck J.F., et al: Transient elastography as a screening tool for liver fibrosis and cirrhosis in a community-based population aged over 45 years. Gut 2011; 60: pp. 977-984
- Berzigotti A.L., and Castera L.: Update on ultrasound imaging of liver fibrosis. J Hepatol 2013; 58: pp. 180-182
85- Elliot B Tapper. Clinical Gastroenterology and hepatology. 2015-01-01. Vol. 13 No 1. Pág 27-36. 2015 AGA Institute
DR: GUILLERMO SEGUNDO PEREZ GONZALEZ Médico Internista Gastroenterólogo Bogotá
Pionero de la Elastografia hepática FibroScan en Colombia
Leave a reply
Leave a reply