LESIONES SUBEPITELIALES GASTRICAS DIAGNOSTICO ENDOSCOPICO Y MANEJO
Las lesiones subepiteliales gástricas (LSEG) son lesiones de intramurales de la pared gástrica que se originan desde la capa muscular propia, submucosa o la muscular propia. Algunas veces son llamados tumores subepiteliales y se encuentran por lo general incidentalmente durante una endoscopia o en un estudio de imagen de corte transversal (TAC o RMN).
Se detectan en el 0.3 % al 2% de las endoscopias digestivas altas y en su mayoría son asintomáticas pero otras pueden manifestarse con sangrado gastrointestinal u obstrucción gástrica dependiendo el tamaño y de la localización dentro del estómago.
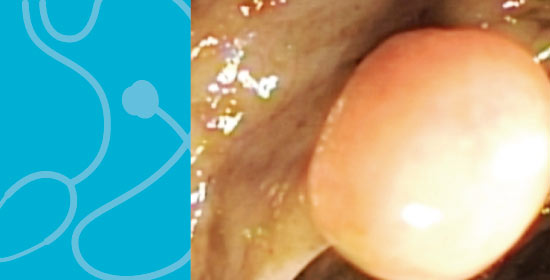
Típicamente se observa como nódulos o elevaciones de la mucosa cubiertas por la mucosa gástrica (signo de tienda de campaña positiva ) y que no desaparecen al cambio de posición ( maniobra endoscópica útil que permite diferenciar de las compresiones extrínsecas )
El diagnóstico diferencial comprende un gran espectro de lesiones benignas (lipomas, páncreas aberrante) o malignas (tumores estromales gastrointestinales o GIST y leiomiosarcomas) estas últimas constituyen el 10-15% de estas lesiones por lo que su identificación y estudio adecuado es importante para el manejo final.
La endoscopia sola es insuficiente para su caracterización debido a que no permite distinguir con exactitud entre lesiones intra o extramulares, tampoco la capa exacta comprometida ni las características intrínsecas de estas lesiones. Además las pinzas de biopsias utilizadas de 5-6 mms a menudo son inadecuadas para tomar muestras de las capas submucosas o muscular propia. Las lesiones de consistencia blandas sugieren lesiones benignas como lipomas y las más duras malignas como los GIST.
El ultrasonido endoscópico (USE) es en la actualidad el examen de primera línea después de una esofagogastroduodenoscopia para estudiar la LSEG dado a que puede aportan información acerca de: tamaño, forma, ecogenicidad, vasculatura, capas de origen, presencia de calcificaciones y de adenopatías vecinas o compromiso extensivo a órganos vecinos. Además el USE puede permitir diferenciar compresión extramural de crecimiento intramural.
En USE la primera y segunda capas corresponden a la mucosa y muscular propia, la tercera capa ala submucosa, la cuarta a la muscular propia y la quinta a la serosa o adventicia.
El USE permite además determinar si la lesión es susceptible de ser resecada por vía endoscópica y la técnica que debe ser utilizada.
En ocasiones se prefiere tomar biopsias con pinzas Jumbo ( más grandes y permiten tomar muestra de tejidos más profundos de las capas submucosas )y con la técnica de biopsias sobre biopsias se puede tener acceso a tejidos más ( 30%-40% en 10 muestras versus 89% en DES o disección endoscópica de la submucosa) no obstante el sangrado después de la primera biopsias dificulta tomar biopsias sobre biopsias; y la cicatriz o fibrosis que puede tener un impacto negativo al intentar una resección futura de la lesión y a su vez puede dificultar la interpretación del USE podría confundir los resultados del USE por lo que se recomienda la secuencia endoscopia, USE y luego si resección .
Se ha descrito la técnica SINK que consiste en realizar una incisión con un bisturí aguja de la mucosa que cubre a la LSE lo cual expone a la lesión y luego utilizando una pinza de biopsias estándar o una yumbo puede aumentar el campo diagnóstico hasta el 92% superando la técnica de FNA (biopsias con aspiración con aguja) que cuya eficacia diagnostica es de solo 26 de 49 pacientes.
Técnicas de biopsias guida por USE: existen la aspiración con aguja fina (FNA o PAAF) o la biopsia con aguja fina (FNB). La biopsia con punción con Trucut (TCB) esta última es técnicamente difícil. Aparte del tipo de aguja y diámetro, otros varios factores contribuyen a las variabilidad del campo diagnóstico y de exactitud con el muestreo guiado con USE. Estos factores incluyen escogencia del tipo de muestreo, técnica de la toma (técnica capilar lenta con estilete, lavado o succión), localización y naturaleza de la lesión, utilización de análisis citopatológico en el sitio de la punción (ROSE), nivel de experiencia del endosonografista y técnica de toma del espécimen. Otros factores son la capacidad de obtener espécimen histológico y la adquisición de tinción con inmunohistoquímica.
La aspiración con aguja fina (FNA o PAAF): fue primero reportada en 1992 y en las últimas décadas se considera el procedimiento de escogencia para acceder y estudiar los tumores sólidos gastrointestinales o acceder a lesiones por fuera del tracto gastrointestinal. Se utiliza para análisis citológico y estudio de bloque celular clave en identificar la mayoría de las LSEG; a pesar de lo extendido de su uso su exactitud es examinador dependiente y varia de 60% al 90%. La USE asociada a la microscopia laser conmofocal aumenta la exactitud diagnóstica (nCLE) realizada a través de una aguja 19 ha sido descrita para adquisición de tejidos guiados.
ROSE (presencia de un cito-patólogo experimentado en el sitio de la punción que revise la calidad de la citología o núcleo).
- La técnica de resección endoscópica de la mucosa EMR, ligadura con banda EMR y ligadura con banda EMR seguida de enucleación. Utiliza una trampa con bisturí aislado ha reportado resección exitosa de lesiones de la muscular propia en un 96.4% (7.1% de perforaciones todas cerradas endoscópicamente). Li et al a descrito resecciones de lesiones de 13 mm con la técnica de enucleación.
- Disección endoscópica submucosa (DES). Es una técnica más demandante que la anterior y ha reportada tasas de resección del 75% al 100% y los efectos adversos serios van del 5% al 10%.
- Tunelización submucosa con resección endoscópica (STER) es una técnica similar a la miotomia per – oral endoscópica (POEM) para la Acalasia . La incisión mucosa es cerrada con clips o suturas, dejando la mucosa intacta al finalizar el procedimiento lo cual evita dejar fugaz del contenido intraluminal al peritoneo. Se han reportado ratas de resección de 97% (meta-análisis) con efectos adversos del 18.3% y perforaciones el 5.6%.
- Resección endoscópica de todas las capas (EFTR). Ofrece un tratamiento alternativo menos invasivo y alterno a la cirugía a la cual se compara en pacientes seleccionados Existe exposición temporal del lumen a la cavidad peritoneal en una de sus variantes en otra se invagina la totalidad de la lesión hacia el lumen luego se sutura de serosa a serosa, se sutura y se reseca. Se ha reportado resección total en el 76% de los casos sin recurrencia evidente a los 3 meses.
GUIAS ACTUALES RCOMENDACIONES Y MANEJO
Las guías publicadas por la ASGE de la conducta a seguir ante la presencia de LSEG es biopsia guida con Ecoendoscopia con aguja fina en los casos asintomáticos para lesiones dependientes en las ecocapas II y III (preferiblemente FNB guida por USE). En caso de no definir diagnóstico se propone seguimiento por USE y repetir la FNB de 3 a 12 meses.
Para las lesiones que aumentan en tamaño u menores de 2 cm se recomienda resección submucosa y ESD, STER o EFTR.
En caso de lesiones localizadas en la cuarta capa la resección endoscópica puede ser considerada para lesiones de 2 a 4 cm de diámetro si un experto está disponible.
Bibliografía:
- Li L, Cristofaro S, Zhou X, et al. Endoscopic submucosal resection: a novel
technique for resection of a small gastric stromal tumor from the muscularis
propria. Am J Gastroenterol 2017; 112:679.
- Meng Y, Li W, Han L, et al. Long-term outcomes of endoscopic submucosal
dissection versus laparoscopic resection for gastric stromal tumors less than
2 cm. J Gastroenterol Hepatol 2017; 32:1693–1697.
- Chun SY, Kim KO, Park DS, et al. Endoscopic submucosal dissection as a
treatment for gastric subepithelial tumors that originate from the muscularis
propria layer: a preliminary analysis of appropriate indications. Surg Endosc
2013; 27:3271–3279.
- He Z, Sun C, Wang J, et al. Efficacy and safety of endoscopic submucosal
dissection in treating gastric subepithelial tumors originating in the muscularis
propria layer: a single-center study of 144 cases. Scand J Gastroenterol
2013; 48:1466–1473.
- Kobara H, Miyaoka Y, Ikeda Y, et al. Outcomes of endoscopic submucosal
dissection for subepithelial lesions localized within the submucosa, including
neuroendocrine tumors: a multicenter prospective study. J Gastrointestin
Liver Dis 2020; 29:41–49.
- Khashab MA, Pasricha PJ. Conquering the third space: challenges and
opportunities for diagnostic and therapeutic endoscopy. Gastrointest Endosc
2013; 77:146–148.
- Meier B, Schmidt A, Glaser N, et al. Endoscopic fullthickness resection of
gastric subepithelial tumors with the gFTRD-system: a prospective pilot study
(RESET trial). Surg Endosc 2020; 34:853–860.
A prospective study evaluating EFTR for gastric SELs.
- Thomas R. McCarty and Marvin Ryou. Endoscopic diagnosis and management of gastric
subepithelial lesions. Current Opinion. Volume 36 Number 6 November 2020.pag 530-537
DR. GUILLERMO SEGUNDO PEREZ GONZALEZ.
Gastroenterólogo-Ecoendoscopista. Bogotá Colombia.
Leave a reply
Leave a reply